
下列有关说法正确的是
A.钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生
B.镀锌铁制品镀层受损后,铁制品比受损前更容易生锈
C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
D.电解法精炼铜时,以粗铜作阳极,粗铜中的所有金属都以离子的形式进入电解质溶液
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
已知常温下CH3COOH和NH3·H2O的电离常数相等,向10ml浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.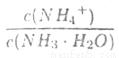 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时c(NH4+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学卷(解析版) 题型:选择题
下列物质的水溶液能导电但属于非电解质的是( )
A.CH3COOH B.Cl2 C.NH4HCO3 D.SO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:选择题
利用催化技术可将汽车尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO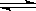 2CO2+ N2。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2+ N2。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) /×10-3 mol·L-1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c(CO) / ×10-3 mol·L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |


 下列说法中,不正确的是
下列说法中,不正确的是
 A.2s内的平均反应速率υ(N2)=1.875×10-4 mol·L-1·s-1
A.2s内的平均反应速率υ(N2)=1.875×10-4 mol·L-1·s-1
 B.在该温度下,反应的平衡常数K=5
B.在该温度下,反应的平衡常数K=5
 C.若将容积缩小为原来的一半,NO转化率大于90%
C.若将容积缩小为原来的一半,NO转化率大于90%
 D.使用催化剂可以通过提高活化分子百分数提高单位时间CO和NO的处理量
D.使用催化剂可以通过提高活化分子百分数提高单位时间CO和NO的处理量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学卷(解析版) 题型:填空题
(1)根据最新“人工固氮”的研究报道,在常温、光照条件下,N2在催化剂(掺有少最Fe2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(g) 2NH3(g)+3/2O2(g) △H =aJ/mol,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
2NH3(g)+3/2O2(g) △H =aJ/mol,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
此合成反应的a________0;△s _________0(填“>”、“<”或“=” )
(2)己知:常温下,0.1mol/L的某酸H2A的pH=4,则该酸为________酸(填“强”或“弱”)。H2A的电离方程式为______________,该滚液中由水电离出的c(H+)=______________。
(3)25℃时,0.1mol/L的HA溶液中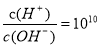 。0.010.1mol/L的BOH溶液pH=12,请回答下列问题:
。0.010.1mol/L的BOH溶液pH=12,请回答下列问题:
①HA是__________(填”强电解质”或“弱电解质”,下同)。
②在加水稀释HA的过程中,随着水量的增加而减小的是__________(填字母)。
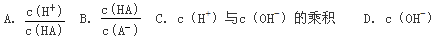
③在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体__________(填“多”“ 少”或“ 相等”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学卷(解析版) 题型:选择题
下列表述中,合理的是( )
A.将水加热,促进水电离,但Kw不变
B.把FeCl2的水溶液加热蒸干井灼烧后可得到Fe2O3晶体
C.用25mL碱式滴定管量取20.00mL 高锰酸钾溶液
D.用水洗净的玻璃棒立即蘸取待测溶液滴到pH试纸中央,半分钟后对照比色卡读出pH值
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次月考化学卷(解析版) 题型:选择题
下列说法不正确的是( )
A.大米富含淀粉 B.加碘食盐含有碘酸钾(KIO3)
C.人体必需的微量元素就是维生素 D.人体必需的微量元素不都是金属元素
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:实验题
二氧化硫常温下为无色有刺激性气味的有毒气体,易液化,易溶于水。某同学设计如下实验方案,对二氧化硫的化学性质进行探究,装置如下图所示。请回答下列问题:

(1)反应结束时烧瓶中Cu由剩余,某同学认为H2SO4也有剩余,他设计了下列实验方案来测定剩余H2SO4的量。经冷却,定量稀释后进行下列实验,能达到的目的是 (填序号)
a.用酸碱中和滴定法测定
b.与足量Zn反应,测量生成H2的体积
c.用pH计测溶液PH值
d.与足量BaCl2溶液反应,称量生成沉淀的质量
(2)装置B的作用是 ,设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式 ,装置D中NaOH全部转化为NaHSO3的标志是____________
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能情况:
I.HSO3-与ClO-刚好反应完; Ⅱ.NaClO不足; Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请你完成下表:(已知酸性:H2SO3>H2CO3>HClO)
实验序号 | 实验操作 | 现象 | 反应的可能情况 |
① | 加入几小块CaCO3固体 | 有气泡产生 | |
② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
③ | 滴加少量溴水,振荡 | Ⅱ | |
④ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液为紫色 |
(4)设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com