
【题目】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。

(1)A装置为CO2的发生装置,其中放置稀盐酸和大理石的仪器名称分别为 ; ,其离子方程式为______________;
(2)B装置可除去A装置中可能挥发出的 (填化学式),其离子方程式为 ,D装置可除去C装置中未反应的 (填名称),其离子方程式为 。
(3)常温下,测得E中生成氧气体积为36.9L (常温下Vm=24.6L/mol),则被还原的过氧化钠质量为 克。
(4)C装置中固体由淡黄色完全变为白色,检验固体成分中有NaOH的实验方案为: 。
【答案】(1)分液漏斗;锥形瓶(1分)
(2)CaCO3+2H+=Ca2++H2O+CO2↑(2分);
HCl(1分);H++HCO3-=H2O+CO2↑(2分);
二氧化碳(1分);2OH-+CO2=CO32-+H2O(2分)
(3)117(2分);(4)取少量固体溶于水,向溶液中滴入过量氯化钙,充分反应后过滤,向滤液中滴入几滴酚酞试液,若变红且不褪色,则证明固体中含有NaOH(3分)
【解析】
试题分析:由实验装置可知,A中碳酸钙与盐酸反应生成二氧化碳气体,B中饱和碳酸氢钠溶液除去挥发的HCl,C中过氧化钠与二氧化碳反应生成氧气、过氧化钠与水反应生成氧气,D中NaOH溶液吸收过量的二氧化碳,E装置为排水法收集氧气,则
(1)A装置中放置稀盐酸和大理石的仪器名称分别为分液漏斗、锥形瓶,其离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑;
(2)由实验装置分析可知B装置的作用为吸收A中挥发出的HCl,反应的离子方程式为H++HCO3-=H2O+CO2↑;D装置的作用是吸收未反应的CO2,反应的离子方程式为2OH-+CO2=CO32-+H2O;
(3)常温下,测得E中生成氧气体积为36.9L(常温下Vm=24.6L/mol),氧气的物质的量是36.9L÷24.6L/mol=1.5mol,则根据方程式2Na2O2+2H2O═4NaOH+O2↑可知被还原的过氧化钠质量为1.5mol,质量是1.5mol×78g/mol=117g;
(4)C装置中固体由淡黄色完全变为白色,有碳酸钠和氢氧化钠生成,氢氧化钠是强碱,所以检验固体成分中有NaOH的实验方案为:取少量固体溶于水,向溶液中滴入过量氯化钙,充分反应后过滤,向滤液中滴入几滴酚酞试液,若变红且不褪色,则证明固体中含有NaOH。


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】微量元素是指在人体内总量不到万分之一,质量总和不到人体质量的千分之一的二十多种元素,这些元素对人体正常代谢和健康起着重要作用。下列元素不是微量元素的是
A.I
B.F
C.H
D.Mn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活.生产密切相关,下列有关叙述正确的是
A.氢氧化铝.小苏打.纯碱均可用作胃酸中和剂
B.古代的陶瓷.水泥.石英玻璃等,都是硅酸盐产品
C.将草木灰(含K2CO3)与NH4Cl混合使用会降低肥效
D.石油的分馏.煤的干馏等物理变化在生产中有着重要的地位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于碳原子成键特点的是( )
A.易失去最外层的电子形成离子
B.最外层电子易与其他原子的外层电子形成共用电子对
C.能够形成单键、双键和三键等多种成键形式
D.每个碳原子最多与其他原子形成4个共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,全部属于纯净物的是( )
A. 福尔马林、酒、醋 B. 苯、汽油、无水酒精
C. 丙三醇、乙醇钠、氯仿 D. 豆油、脂肪、四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol·L﹣1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
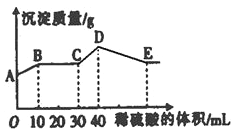
A.AB段发生反应的离子方程式为:Ba2++SO42—═BaSO4↓
B.E点对应横坐标稀硫酸的体积为70 mL
C.D点表示的沉淀的化学式为Al(OH)3、BaSO4
D.E点沉淀比A点沉淀质量大2.33g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.苯只能发生取代反应,乙烯只能发生加成反应
B.甘氨酸和丙氨酸混合物脱水成肽,最多可生成4种二肽
C.C4H9OH有4种同分异构体
D.C3H6和C4H8一定是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ag2SO4的Ksp 为2.0×10-5,将适量Ag2SO4固体溶于水中配成100 mL饱和溶液,该过程中Ag+和SO42-浓度随时间变化关系如图[饱和Ag2SO4溶液中c(Ag+)=0.034 mol·L-1]。若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4 溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是( )
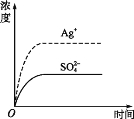
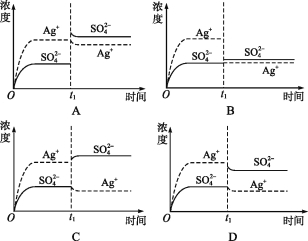
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com