
| A. | 2:1 | B. | 3:2 | C. | 5:2 | D. | 5:1 |
分析 在每个氯化钠晶胞中分别含有4个Na+、Cl-,离子总数为8,在冰晶石晶胞中,AlF63-占据的位置相当于NaCl晶胞中C1-占据的位置,所以冰晶石晶胞中AlF63-的数目为4,根据冰晶石的化学式(Na3AlF6)可知,晶胞中钠离子数为12,所以冰晶石晶胞中原子总数为40.
解答 解:在每个氯化钠晶胞中分别含有4个Na+、Cl-,离子总数为8,在冰晶石晶胞中,AlF63-占据的位置相当于NaCl晶胞中C1-占据的位置,所以冰晶石晶胞中AlF63-的数目为4,根据冰晶石的化学式(Na3AlF6)可知,晶胞中钠离子数为12,所以冰晶石晶胞中原子总数为40,所以冰晶石晶胞中含有的原子数与食盐晶胞中含有的原子数之比为40:8=5:1,
故选D.
点评 本题考查晶胞计算,侧重考查学生分析计算、空间想象及获取信息解答问题能力,正确利用题给信息是解本题关键,熟练掌握氯化钠、氯化铯晶胞结构特点,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:解答题
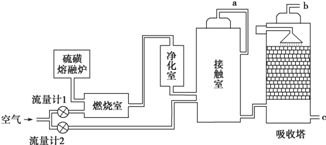
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
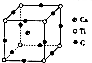 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.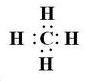 ,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.
,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭 |
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A-F) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
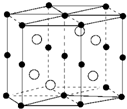
| A. | 锰价电子排布为3d74s0 | B. | Bi是d区金属 | ||
| C. | 该晶体的化学式为MnBi | D. | 该合金堆积方式是简单立方 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com