
 ¢ń”¢Čē¹ūÅäÖĘ3mol/LµÄNaOHČÜŅŗ500mL£¬Šč³ĘĮæNaOH¹ĢĢå60.0g£®
¢ń”¢Čē¹ūÅäÖĘ3mol/LµÄNaOHČÜŅŗ500mL£¬Šč³ĘĮæNaOH¹ĢĢå60.0g£®·ÖĪö I”¢øł¾Żn=cVŗĶm=nMĄ“¼ĘĖć£»
£Ø1£©øł¾ŻÅäÖĘ²½ÖčŹĒ¼ĘĖć”¢³ĘĮ攢Čܽā”¢ĄäČ“”¢ŅĘŅŗ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČ”¢×°ĘæĄ“·ÖĪöŠčŅŖµÄŅĒĘ÷£»
£Ø2£©øł¾Żc=$\frac{n}{V}$²¢½įŗĻČÜÖŹµÄĪļÖŹµÄĮænŗĶČÜŅŗµÄĢå»żVµÄ±ä»ÆĄ“½ųŠŠĪó²ī·ÖĪö£»
II”¢£Ø1£©CO2ÓėNaOH·“Ó¦æÉÉś³ÉNa2CO3»ņNaHCO3£¬¶žÕßČÜŅŗ¶¼³Ź¼īŠŌ£»
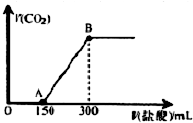
£Ø2£©¼ÓČėŃĪĖį1500mLŹ±æŖŹ¼Éś³ÉĘųĢ壬µ±¼ÓČėŃĪĖį300mLŹ±²»ŌŁ²śÉśĘųĢ壬O”śA¶Ī·¢Éś·“Ó¦£ŗNa2CO3+HClØTNaCl+NaHCO3£¬A”śB¶Ī·¢ÉśNaHCO3+HClØTNaCl+H2O+CO2”ü£¬¶ųO”śA¶ĪĻūŗĵÄŃĪĖįĪŖA”śBĻūŗĵÄŃĪĖįµÄ¶ž±¶£¬£®
¢Łøł¾ŻĶ¼ĻóæÉÖŖ£¬¼ÓČėµÄŃĪĖįŅ»æŖŹ¼ĪŽĘųĢåÉś³É£¬¹ŹæÉĶĘÖŖµ„Ņ»µÄČÜÖŹ£»
¢ŚO”śA¶Ī·¢Éś·“Ó¦£ŗNa2CO3+HClØTNaCl+NaHCO3£»
¢Ūøł¾ŻAB¶Ī·“Ó¦Ą“·ÖĪö£»BµćČÜŅŗÖŠČÜÖŹĪŖNaCl£¬ÓÉÄĘĄė×ÓŹŲŗćæÉÖŖn£ØNaCl£©=n£ØNaOH£©£¬½ų¶ų¼ĘĖćĀČ»ÆÄʵÄÅØ¶Č£®
½ā“š ½ā£ŗI”¢ÅäÖĘ3mol/LµÄNaOHČÜŅŗ500mL£¬ĖłŠčµÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæn=cV=3mol/L”Į0.5L=1.5mol£¬ÖŹĮæm=nM=1.5mol”Į40g/mol=60.0g£¬¹Ź“š°øĪŖ£ŗ60.0£»
£Ø1£©øł¾ŻÅäÖĘ²½ÖčŹĒ¼ĘĖć”¢³ĘĮ攢Čܽā”¢ĄäČ“”¢ŅĘŅŗ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČ”¢×°ĘææÉÖŖĖłŠčµÄŅĒĘ÷ÓŠ500mLČŻĮæĘæŗĶ½ŗĶ·µĪ¹Ü”¢ĮæĶ²”¢ÉÕ±”¢²£Į§°ō£¬¹Ź“š°øĪŖ£ŗ500mLČŻĮæĘ棻
£Ø2£©Čē¹ūŌŚ¶ØČŻŹ±ŃöŹÓ£¬ŌņČÜŅŗĢå»ż½«Ę«“ó£¬ČÜŅŗÅØ¶Č½«Ę«Š”£»Čō¶ØČŻŹ±ŅŗĆęøßÓŚæĢ¶ČĻßÓ¦²ÉČ”µÄ“ėŹ©ŹĒÖŲŠĀÅäÖĘ£¬¹Ź“š°øĪŖ£ŗĘ«Š”£¬ÖŲŠĀÅäÖĘ£»
II”¢£Ø1£©CO2ÓėNaOH·“Ó¦æÉÉś³ÉNa2CO3»ņNaHCO3£¬¶žÕßČÜŅŗ¶¼³Ź¼īŠŌ£¬ŌņČē¹ūŹĒµ„Ņ»³É·Ö£¬æÉÄÜŹĒNa2CO3»ņNaHCO3£¬
¹Ź“š°øĪŖ£ŗNa2CO3»ņNaHCO3£»
£Ø2£©¼ÓČėŃĪĖį200mLŹ±æŖŹ¼Éś³ÉĘųĢ壬µ±¼ÓČėŃĪĖį300mLŹ±²»ŌŁ²śÉśĘųĢ壬ĪŽĘųĢå²śÉśŗĶÉś³ÉĘųĢå¶ĪĖłŠčµÄŃĪĖįµÄĢå»ż±ČĪŖ1£ŗ1£¬æÉÖŖČÜŅŗÖŠµÄČÜÖŹĪŖNa2CO3£¬O”śA¶Ī·¢Éś·“Ó¦£ŗNa2CO3+HClØTNaCl+NaHCO3£¬A”śB¶Ī·¢ÉśNaHCO3+HClØTNaCl+H2O+CO2”ü£®
¢Łøł¾ŻĶ¼ĻóæÉÖŖ£¬¼ÓČėŃĪĖį200mLŹ±æŖŹ¼Éś³ÉĘųĢ壬µ±¼ÓČėŃĪĖį300mLŹ±²»ŌŁ²śÉśĘųĢ壬ĪŽĘųĢå²śÉśŗĶÉś³ÉĘųĢå¶ĪĖłŠčµÄŃĪĖįµÄĢå»ż±ČĪŖ1£ŗ1£¬æÉÖŖČÜŅŗÖŠµÄČÜÖŹĪŖNa2CO3£¬¹ŹæÉĶĘÖŖµ„Ņ»µÄČÜÖŹĪŖNa2CO3£¬¹Ź“š°øĪŖ£ŗNa2CO3£»
¢ŚO”śA¶Ī·¢Éś·“Ó¦£ŗNa2CO3+HClØTNaCl+NaHCO3£¬¹ŹĄė×Ó·½³ĢŹ½ĪŖ£ŗCO32-+H+ØTHCO3-£¬¹Ź“š°øĪŖ£ŗCO32-+H+ØTHCO3-£»
¢ŪA”śB¶Ī·¢ÉśNaHCO3+HClØTNaCl+H2O+CO2”ü£¬ĻūŗÄŃĪĖįµÄĢå»żĪŖ150mL£¬ĪļÖŹµÄĮæn=CV=1mol/L”Į0.15L=0.15mol£¬ÉčÉś³ÉµÄ¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖxmol£¬ŌņÓŠ£ŗ
NaHCO3+HClØTNaCl+H2O+CO2”ü
1 1
0.15mol xmol
¹ŹÓŠ£ŗ$\frac{1}{0.15mol}=\frac{1}{xmol}$
½āµĆx=0.15mol£®
0.15mol¶žŃõ»ÆĢ¼ŌŚ±źæöĻĀµÄĢå»żV=nVm=0.15mol”Į22.4L/mol=3360mL£»
BµćČÜŅŗÖŠČÜÖŹĪŖNaCl£¬ÓÉÄĘĄė×ÓŹŲŗćæÉÖŖn£ØNaCl£©=n£ØNaOH£©=0.1L”Į3mol/L=0.3mol£¬ŌņNaClµÄĪļÖŹµÄĮæÅØ¶ČŹĒ£ŗ$\frac{0.3mol}{0.1L+0.3L}$=0.75mol/L£¬
¹Ź“š°øĪŖ£ŗ3360mL£»0.75mol/L£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬¹Ų¼üŹĒøł¾ŻĶ¼Ļó·ÖĪöø÷½×¶Ī·¢ÉśµÄ·“Ó¦£¬×¢Ņā¼ĘĖć¹ż³ĢÖŠŹŲŗćĖ¼ĻėµÄÓ¦ÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²£Į§øÖŹĒø“ŗĻ²ÄĮĻ | B£® | ĀĮŹĒŗŚÉ«½šŹō²ÄĮĻ | ||
| C£® | ŹÆÓ¢ŹĒ°ėµ¼Ģå²ÄĮĻ | D£® | Ė®ÄąŹĒŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| V£ØAgNO3£©/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņNaHSO4ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗÖĮÖŠŠŌ£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O | |
| B£® | Ļņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČė×ćĮæCO2£ŗ2Na++CO32-+CO2+H2OØT2NaHCO3”ż | |
| C£® | ĻņCa£ØHCO3£©2ČÜŅŗÖŠ¼ÓČė×ćĮæCa£ØOH£©2ČÜŅŗ£ŗCa2++HCO3-+2OH-ØTCaCO3”ż+CO32-+2H2O | |
| D£® | Ļņ“ĪĀČĖįČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£ŗH++OH-ØTH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
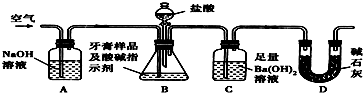
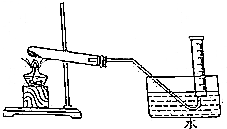 ĪŖŃéÖ¤MnO2ŌŚKClO3ŹÜČČ·Ö½āÖĘO2µÄ·“Ó¦Ē°ŗóÖŹĮæ²»±ä£¬Ä³ŠĖȤŠ”×éĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĮĖČēĻĀŹµŃé£ŗ
ĪŖŃéÖ¤MnO2ŌŚKClO3ŹÜČČ·Ö½āÖĘO2µÄ·“Ó¦Ē°ŗóÖŹĮæ²»±ä£¬Ä³ŠĖȤŠ”×éĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĮĖČēĻĀŹµŃé£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æĻ¶ØÓŠSO2”¢NO”¢O2 | B£® | æĻ¶ØƻӊC12”¢O2ŗĶNO2 | ||
| C£® | æÉÄÜÓŠCl2ŗĶO2 | D£® | æĻ¶ØÖ»ÓŠNO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
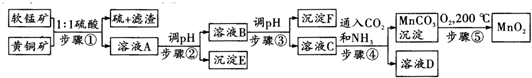
| ³ĮµķĪļ | Cu£ØOH£©2 | Fe£ØOH£©3 | Mn£ØOH£©2 | Fe£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 4.2 | 1.5 | 7.3 | 6.4 |
| ĶźČ«³ĮµķpH | 6.7 | 3.2 | 9.8 | 9.0 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com