
某工厂废弃的钒渣中主要含V2O5、VOSO4、K2SO4、SiO2等,现从该钒渣回收V2O5的工艺流程示意图如下:
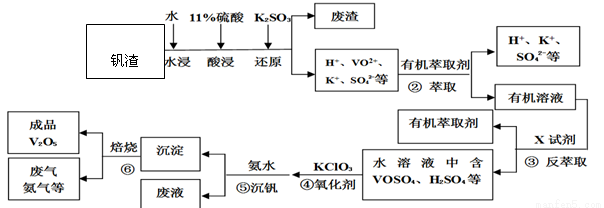
(已知:沉淀为(NH4)2V6O16,全钒液流储能电池是利用不同价态离子对氧化还原反应来实现化学能和电能相互转化的装置,②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂)。
R2(SO4)n(水层)+2nHA(有机层)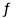 2RAn(有机层) + nH2SO4(水层)
2RAn(有机层) + nH2SO4(水层)
回答下列问题:
(1)(NH4)2V6O16中钒(V)的化合价为 ,①中产生的废渣的主要成分是 。
(2)工艺中反萃取所用的X试剂为 。
(3)为提高②中萃取效率,应采取的措施是 。
(4)请完成④中的反应离子方程式:
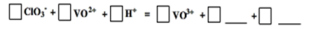
(5)成品V2O5可通过铝热反应来制取金属钒,写出该反应的化学方程式: 。
(6)将两个全钒液流储能电池串联后作为电源,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,装置如下:
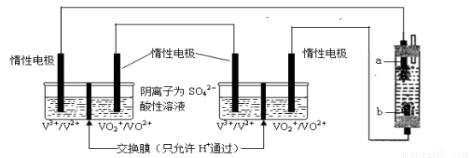
b为电解池的 极,全钒液流储能电池正极的电极反应式为 ;
若通过消毒液发生器的电子为0.2 mol,则消毒液发生器中理论上最多能产生 gNaClO。
(除标记外每空2分,共15分)
(1)+5 (1分) SiO2(名称也可,1分)
(2)稀硫酸(化学式也可)
(3)加入碱(具体碱均可)中和硫酸使平衡正移、多次连续萃取(写“多次连续萃取”也得2分;写“加入Zn、Fe等、弱酸强碱盐” 也得2分;写“增大萃取剂的加入量”给1分;写“增大萃取剂浓度”不得分)
(4)1ClO3—+6VO2++6H+=6VO3++1Cl—+3H2O
(有错计0分,“1”未写本次不扣分)
(5) 10Al+3V2O5 6V+5Al2O3
6V+5Al2O3
(6)阳(1分) VO2++ e-+2H+=VO2++H2O 7.45
【解析】
试题分析:(1)根据化合物中正负化合价代数和为0可判断(NH4)2V6O16中N为-3、H为+1、O为-2价,则钒(V)的化合价为+5价;根据流程图可知,只有二氧化硅不溶于硫酸,所以废渣的主要成分是SiO2;
(2)从流程图中可看出,加入反萃取剂X后,又得到有机萃取剂和含V元素的混合液,根据R2(SO4)n(水层)+2nHA(有机层)  2RAn(有机层) + nH2SO4(水层)可知,该平衡应逆向进行,所以加入的X是硫酸;
2RAn(有机层) + nH2SO4(水层)可知,该平衡应逆向进行,所以加入的X是硫酸;
(3)为提高②中萃取效率,使上述平衡正向移动,则应加入碱性物质,同时多次萃取也可增大萃取效率;
(4)V元素的化合价从+4价升高到+5价,则氯酸根离子中的Cl元素的化合价从+5价应降低到-1价,同时根据元素守恒,则产物中还有水生成,所以产物的空白为Cl-和H2O;再根据得失电子守恒,VO2+和VO3+的系数是6,氯酸根离子和氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3;
(5)铝热反应是单质Al与金属氧化物的置换反应,所以用Al与五氧化二钒反应生成氧化铝和钒的化学方程式是10Al+3V2O5 6V+5Al2O3;
6V+5Al2O3;
(6)电解饱和食盐水时,氯气在阳极产生,氢氧化钠再阴极产生,若使氯气被全部吸收,则氯气在下端,所以b极产生氯气,则b极为阳极;全钒液流储能电池正极发生还原反应,V元素的化合价降低,与b相连的为正极,所以正极反应式是VO2++ e-+2H+=VO2++H2O;产生氯气的电极反应式为2Cl--2e-=Cl2↑,氯气与氢氧化钠反应的离子方程式是Cl2+2 OH-= Cl-+ ClO-+ H2O,当电路中通过0.2mol电子时,产生氯气的物质的量是0.1mol,则消毒液发生器中理论上最多能产生0.1molNaClO,其质量是7.45g。
考点:考查对流程的分析,元素化合价的判断,电化学反应原理的应用
考点分析: 考点1:原电池 考点2:电解池 考点3:物质的分离、除杂和提纯 考点4:物质的检验和鉴别 试题属性

科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
下列有关溶液组成的描述合理的是
A.无色溶液中可能大量存在Al3+、NH4+、Cl-、OH-
B.酸性溶液中可能大量存在Na+、ClO-、SO42-、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3-
D.红色溶液中可能大量存在Fe3+、K+、Cl-、SCN-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省六校高三3月联考理综化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2 剧烈化合并发生爆炸。则下列判断正确的是
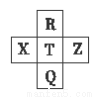
A.元素R对应气态氢化物的相对分子质量实际测量值往往比理论上要大的多,这可能和氢键有关
B.由于键能EH-R>EH-T,故元素R、T对应气态氢化物的沸点:HR>HT
C.R与Q的电子数相差16
D.最高价氧化物对应的水化物的酸性:X<T<Q
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)氢气是一种理想的“绿色能源”,利用氢能需要选择合适的储氢材料。目前正在研究和使用的储氢材料有镁系合金、稀土系合金等。
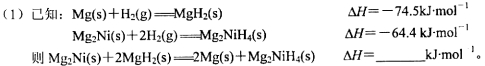
(2)储氢材料Mg(AlH4)2在110~200℃的反应为:Mg(AlH4)2==MgH2+2Al+3H2↑。
反应中每转移3mol电子时,产生的H2在标准状况下的体积为__________L。
(3)镧镍合金在一定条件下可吸收氢气形成氢化物: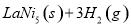
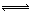 LaNi5H6(s)
LaNi5H6(s)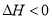 ,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
a.增加LaNi5H6(s)的量
b.升高温度
c.减小压强
d.使用催化剂
(4)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
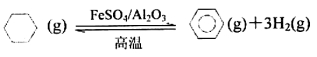
①某温度下,向恒容密闭容器中加入环己烷,起始浓度为amol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=____________(用含a、b的代数式表示)。
②一定条件下,下图装置可实现有机物的电化学储氢(忽略其它有机物)。

A是电源的______极(填“正”或“负”);电解过程中产生的气体F为_____(填化学式):电极D上发生的电极反应为__________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:选择题
化学与能源开发、环境保护、生产生活等密切相关。下列叙述错误的是
A.光催化水制氢比电解水制氢更节能环保
B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
C.开发利用可再生能源,可减少化石燃料的使用
D.改进汽车尾气净化技术,可减少大气污染物的排放
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
-C3H7和-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有
A.10种 B.15种 C.30种 D.36种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州五校高三上学期摸底联考化学试卷(解析版) 题型:填空题
(15分)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。
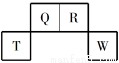
(1)T的原子结构示意图是______。用化学方程式表示工业上常用于冶炼T单质的原理是_________。
(2)与W同主族的某元素,其氢化物分子中含有18个电子,该分子中的共价键类型是________ 。
(3)元素的非金属性:Q________W(填“强于”或“弱于”),结合方程式简述其原因是__________ _。
(4)元素X与T同周期,且在该周期中原子半径最大,请写出X的最高价氧化物的水化物与T的最高价氧化物的水化物反应的离子方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州五校高三上学期摸底联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.酸、碱、盐都是电解质 B.电解质都是易溶于水的物质
C.氧化物都是电解质 D.氢化物都不是电解质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.HOCH2COOH的缩聚物是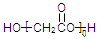
B.乙醛和丙烯醛( )不是同系物
)不是同系物
C.已知甲醛分子中各原子共平面,则丙烯醛所有原子一定共平面
D.结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子的单体是1,3-丁二烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com