
| A. | 煤的干馏和石油的分馏均属于化学变化 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 用油料作物生产的生物柴油成分与石油中提取的柴油成分相同 | |
| D. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 |
分析 A.有新物质生成的是化学变化;
B.由同一种元素组成的性质不同的几种单质,叫做该元素的同素异形体;
C.生物柴油主要成分是油脂;
D.葡萄糖注射液是溶液.
解答 解:A.石油的分馏属物理变化,因为石油的分馏是利用石油中各种成分沸点不同将其分离的一种方法,没有新物质生成,所以是物理变化,煤的干馏是复杂的物理化学变化,故A错误;
B.14C与12C是原子,不是单质,故B错误;
C.生物柴油主要成分是油脂,柴油主要成分是烃,故C错误;
D.葡萄糖注射液是溶液,不属于胶体,丁达尔现象是胶体具有的性质,故D正确.
故选D.
点评 本题考查分馏与干馏的区别、同位素和同素异形体、有机物的性质以及胶体和溶液的区别等,题目难度不大,注意相关基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | K +、Na +、SO42-、S2O32- | B. | NH4+、Mg 2+、SO42-、Cl - | ||
| C. | Na +、K +、HCO3-、Cl - | D. | K +、Na +、AlO2-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 500℃时,在催化剂存在条件下,分别将2mol SO2和1mol O2置于恒压容器I和恒容容器II中(两容器起始容积相同),充分反应,二者均达到平衡后:
500℃时,在催化剂存在条件下,分别将2mol SO2和1mol O2置于恒压容器I和恒容容器II中(两容器起始容积相同),充分反应,二者均达到平衡后:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH4 | CH3-CH3 | CH2═CH2 |
| 物质的量分数 | 20% | 30% | 50% |
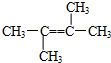 所示,
所示,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子:12C | B. | HClO的结构式:H-Cl-O | ||
| C. | 镁离子的结构示意图: | D. | 乙酸的分子式:C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自行车的钢圈镀铬 | B. | 室外的铁制水管外面刷油漆 | ||
| C. | 电线外面包上一层塑料 | D. | 地下钢管连接铜块防腐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com