
纳米材料的表面微粒的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为( )
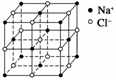
A.7∶8 B.13∶14
C.25∶26 D.26∶27
科目:高中化学 来源: 题型:
如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
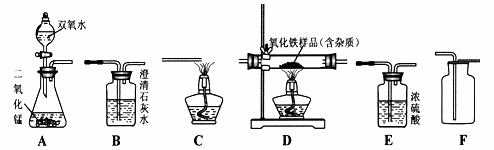
(1)欲在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为 (填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为 。
(2)欲用足量纯净的一氧化碳气体测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:纯净的一氧化碳气体 →D→B→C。
①仪器C的作用是 。
②仪器D中发生的化学反应方程式为
③反应完全后,计算氧化铁样品的纯度时, 小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”。小丽同学通过称量发现二者质量并不相等。请你分析写出仪器D中减少的是 ________的质量,而仪器B中增加的是 _________的质量。
小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”。小丽同学通过称量发现二者质量并不相等。请你分析写出仪器D中减少的是 ________的质量,而仪器B中增加的是 _________的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充入1 mol A、3 mol B,此时两容器体积均为
500 mL,温度为T ℃,保持温度不变发生反应:A(g)+3B(g) 2C(g)+D(s)
2C(g)+D(s)
ΔH<0
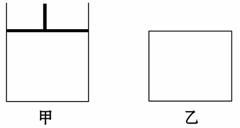
(1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是_______。
A.混合气体的总质量不随时间改变
B.2v正(C)=3v逆(B)
C.A、B转化率相等
D.物质D的质量不随时间改变
(2)2 min后甲容器中反应达到平衡,测得C的浓度为2 mol·L-1,此时容器的体积为________mL,B的转化率α甲(B)为________。
(3)乙容器中反应达到平衡所需要的时间____2 min(填“>”“<”或“=”,下同),B的转化率α乙(B)____α甲(B)。
(4)其他条件不变,甲中如果从逆反应方向开始反应建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加入C的物质的量n(C)为_________mol,加入D的物质的量n(D)应该满足的条件为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应水化物的酸性从左到右依次增强
D.第2周期元素随族序数的递增其最高化合价也递增
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是短周期的四种主族元素,它们的原子序数依次增大,四种元素中只有C是金属元素,A与C的最外层电子数相等,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍。试推断:
(1)写出A、B、C、D的元素符号:
A__________、B__________、C__________、D__________;
(2)写出D元素原子的基态电子排布式________________;
(3)B、C、D三元素的第一电离能由大到小的顺序为__________(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
纳米材料是指颗粒的三维限度中的任一维在1 nm~100 nm范围的材料,纳米技术所带动的技术革命及其对人类的影响,远远超过电子技术。下列关于纳米技术的叙述不正确的是( )
A.将“纳米材料”分散到液体分散剂中可制得液溶胶
B.用纳米级金属颗粒粉剂作催化剂可加快反应速率,提高反应物的平衡转化率
C.用纳米颗粒粉剂做成火箭的固体燃料将有更大的推动力
D.银器能抑菌、杀菌,纳米银粒子植入内衣织物中,有奇异的抑菌、杀菌效果
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质特殊聚集状态结构的叙述中,错误的是( )
A.等离子体的基本构成微粒的排列是带电的离子和电子及不带电的分子或原子
B.非晶体基本构成微粒的排列是长程无序和短程有序的
C.液晶内部分子沿分子长轴方向有序排列,使液晶具有各向异性
D.纳米材料包括纳米颗粒与颗粒间的界面两部分,两部分都是长程有序的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是
A.乙烯和苯都能使溴水褪色,褪色的原理相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
D.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)自从1962年首次合成了第一个稀有气体的化合物XePtF6以来,人们又相继发现了氙气的一系列化合物如XeF2、XeF4等。巴特列为开拓稀有气体化学作出了历史性贡献。
①请根据XeF4的结构示意图(图1)判断这个分子是 (填极性分子或非极性分子)。
②XeF2晶体是一种无色晶体,图2为它的晶胞结构图。XeF2晶体属于哪种类型的晶体__________;
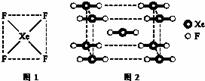
③一个XeF2晶胞中实际拥有XeF2_______个。
(2)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为 ,1 mol乙醛分子中含有的σ键的数目为 。乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com