
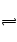 10Ca2+(aq)+6PO43-(aq)+2OH-(aq),已知25℃时Ksp[Ca10(PO4)6(OH)2]="2.35" ×10-59, Ksp[Ca10(PO4)6F2]=7.1× 10-61,Ksp[CaCO3]="5" ×10-9,Ksp[CaF2]=4×10-11,下列说法不正确是( )
10Ca2+(aq)+6PO43-(aq)+2OH-(aq),已知25℃时Ksp[Ca10(PO4)6(OH)2]="2.35" ×10-59, Ksp[Ca10(PO4)6F2]=7.1× 10-61,Ksp[CaCO3]="5" ×10-9,Ksp[CaF2]=4×10-11,下列说法不正确是( )| A.口腔内残留食物会发酵使口腔呈酸性,所以饭后、睡前应该要漱口 |
| B.饮用水中氟元素含量较低的地区使用含氟牙膏可有效防止龋齿 |
| C.25℃时饱和CaCO3溶液和饱和CaF2溶液相比,后者c(Ca2+)较大 |
| D.25℃时,在CaCO3悬浊液中加入NaF溶液后,CaCO3不可能转化为CaF2 |
科目:高中化学 来源:不详 题型:单选题
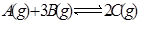 达到平衡的标志的是( )
达到平衡的标志的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| B.工业合成氨时选择铁做催化剂能极大加快反应速率 |
| C.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
| D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g) ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是
2SO3(g) ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是| A.第一次实验平衡时反应放出的热量为98.3kJ |
| B.第一次实验平衡时SO2的转化率比第二次实验平衡时SO2的转化率大 |
| C.第二次实验达平衡时SO3的体积分数大于2/9 |
| D.两次实验平衡时,SO3的浓度相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g) + qD(g)的平衡常数为K,下列说法正确的是
pC(g) + qD(g)的平衡常数为K,下列说法正确的是| A.平衡常数发生变化,化学平衡必发生移动 |
| B.化学平衡发生移动,平衡常数必发生变化 |
| C.反应物的转化率越大,达到平衡时,K值越大 |
| D.温度越高,达到平衡时,K值越大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
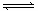 C(g)+D(g)达到平衡的标志是( )
C(g)+D(g)达到平衡的标志是( )| A.压强不变 | B.每分钟A的减少量等于D的增加量的两倍 |
| C.B物质的浓度不变 | D.A物质的百分含量不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
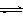 CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol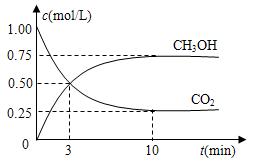
A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1mol CO2和3mol H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  ΔH1
ΔH1 CH3OH(g) ΔH2
CH3OH(g) ΔH2 。
。 平衡常数(K)
平衡常数(K) | 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com