
| A、胶体是带电的,溶液是电中性的 |
| B、向煮沸的1mol/LNaOH溶液 中滴加FeCl3饱和溶液得Fe(OH)3胶体 |
| C、依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
| D、向污水投放明矾,能生成凝聚悬浮物的胶体 |


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:

| A、该硫酸的物质的量浓度为9.2mol?L-1 |
| B、1molZn与足量的该硫酸反应产生4g氢气 |
| C、配制200mL4.6mol?L-1的稀硫酸需取该硫酸50mL |
| D、等质量的水与该硫酸混合所得溶液的物质的量浓度大于9.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B |
| C | D |
| A、若D是双原子分子,则单质的熔点大小关系为D>B>A |
| B、若C单质为原子晶体,且具有金属光泽.则B的氢化物分子式为BH3 |
| C、若A元素原子最外层只有1个电子,则D单质既能与酸又能与碱溶液反应 |
| D、A和C可形成CA3型化合物,则一定能形成CA2型化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Al3+、NO3-、Cl- |
| B、K+、Na+、Cl-、AlO2- |
| C、Fe2+、K+、NO3-、Cl- |
| D、Na+、HCO3-、K+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在氧化还原反应中,一定是一种元素被氧化另一种元素被还原 |
| B、某元素由化合态转化为游离态,这种元素可能被氧化也有可能被还原 |
| C、氧化还原反应中,还原剂失电子越多,还原性越强 |
| D、氧化还原反应中,较难失电子的原子,一定容易得到电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、乙炔氢氯化法:CH≡CH+HCl
| ||||
B、乙烯直接氯化法:CH2=CH2+Cl2
| ||||
| C、乙烯氯化裂解法:CH2=CH2+Cl2→CH2Cl-CH2Cl CH2Cl-CH2Cl
| ||||
D、乙烯氯化平衡法:2CH2=CH2+4HCl+O2
2CH2Cl-CH2Cl
|
查看答案和解析>>
科目:高中化学 来源: 题型:
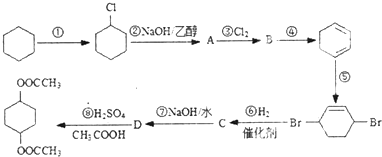
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5mol |
| B、1mol |
| C、0.5mol |
| D、0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2+、Al3+ |
| B、Fe2+、Fe3+ |
| C、Fe3+、Al3+ |
| D、Fe2+、Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com