
| A. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照条件下和点燃条件下的△H不同 | |
| B. | 常温下反应2A(s)+B(g)═2C(g)+D(g)不能自发进行,则反应的焓变一定大于零 | |
| C. | 需要加热的化学反应,生成物的总能量一定高于反应物的总能量 | |
| D. | 等质量的硫粉分别在空气、氧气中燃烧,放出热量多的是硫粉在氧气燃烧 |
分析 A.反应的热效应只与始态、终态有关,与过程无关;
B.反应自发进行的判断依据是△H-T△S<0;
C.生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,与反应条件无关;
D.反应热只与反应物的量及其状态有关.
解答 解:A.反应的热效应只与始态、终态有关,与过程无关,所以同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同,故A错误;
B.反应自发进行的判断依据是△H-T△S<0自发,△H-T△S>0不自发,已知常温下,反应2A(s)+B(g)=2C(g)+D(g)为熵增大的反应即△S>0,若△H-T△S>0,则反应的焓变一定大于零,故B正确;
C.生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,与反应条件无关,所以需要加热的化学反应,不一定是生成物的总能量高于反应物的总能量,故C错误;
D.反应热只与反应物的量及其状态有关,所以等质量的硫粉分别在空气、氧气中燃烧,放出热量一样多,故D错误;
故选B.
点评 本题考查化学变化特征、反应自发性的判断、能量转化形式等,比较基础,注意对基础知识的理解掌握.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:解答题
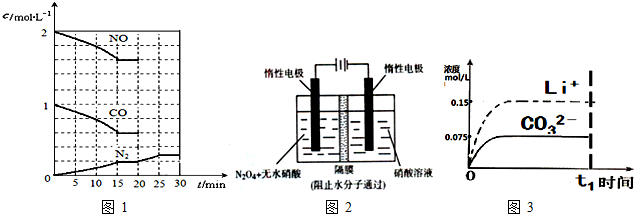 (填“向左”、“向右”或“不”).
(填“向左”、“向右”或“不”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②③ | C. | ②③④⑥ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可加入硫酸、氢氧化钾等强电解质以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 放电过程中,电池正极材料的质量不变 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在此反应中硝酸体现强氧化性,全部被还原 | |
| B. | 向反应后的溶液中再加入金属铁,不再发生化学反应 | |
| C. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:4 | |
| D. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例.在250mL圆底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解.滴入4〜6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图):
化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例.在250mL圆底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解.滴入4〜6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com