
 ;
; ;BCD;
;BCD;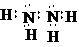 ;
;
| ||
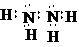 ;2NH4Cl+Ca(OH)2
;2NH4Cl+Ca(OH)2
| ||


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
| 实验操作 | 实验现象 | 结论及解释 |
| ①取少量NaBr 溶液于试管中,滴加 ②再加入少量CCl4,振荡,静置. | ①溶液由无色变为橙黄色. ②溶液分层, | 氧化性:Z 单质>Br2 离子方程式 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.2mol?L-1?min-1 |
| B、1.0 mol?L-1?min-1 |
| C、0.5 mol?L-1?min-1 |
| D、0.4 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5的颗粒物,分散在空气中可形成胶体 |
| B、汽车尾气不仅能形成光化学污染还能破坏臭氧层 |
| C、对废旧电池进行回收处理主要为了防止重金属污染水源 |
| D、富含氮、磷的生活污水不能排放到河中,但可以直接用于农田的灌溉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com