
化合物A为一种常见金属元素与一种常见非金属元素组成的化合物,阳离子与阴离子的个数比为2:3。K为常见固态非金属单质,J为常见气态单质。其余为化合物,其中I、F在常温下为液态,C、D为刺激性气体,H无色无味气体,B为白色胶状沉淀,L为氯碱工业中的常见产品。F的浓溶液与K加热可生成D和H。(部分生成物未标出)
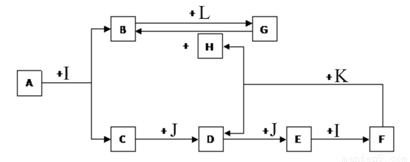
(1)写出下列物质的化学式:E J
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:_______________________
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式_____________
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是
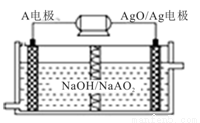
A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=AO2-+2H2O
D.正极的电极反应式为:O2+2H2O+4e-=4OH-
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源:2015-2016学年山东省济宁市高一上12月阶段测化学试卷(解析版) 题型:选择题
X、Y、Z、W有如图所示的转化关系,则X、Y可能是
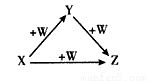
①C、CO ②AlCl3、Al(OH)3 ③Fe、FeCl3 ④Na2CO3、NaHCO3
A.只有①② B.只有③④ C.只有①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第五次模拟理综化学试卷(解析版) 题型:填空题
【选修2:化学与技术】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌。某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为___________。
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的____________________操作。
(3)浸出液“净化”过程中加入的主要物质为___________ ,其作用是__________________。
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气体是________。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生的主要反应的离子方程式为___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
相同质量的下列各烃,完全燃烧后消耗氧气最多的是( )
A.甲烷 B.乙烷 C.乙烯 D.乙炔
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省衡水市高一上第四次月考化学试卷(解析版) 题型:选择题
下列各组物质混合后,不能生成氢氧化钠的是( )
A.钠和水 B.过氧化钠和水
C. 氢氧化钙溶液和碳酸钠溶液 D.氢氧化钙溶液和氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2016届江西师大附中、临川一中高三上第一次联考化学试卷(解析版) 题型:选择题
下列关于物质的分类或变化说法正确的是
A.稀硫酸、NaCl溶液是实验室常见的强电解质
B.二氧化氮经加压凝成无色液体为物理变化
C.Na2O·SiO2是一种简单的硅酸盐,可溶于水
D.溴水滴入植物油中振荡褪色,说明溴被植物油从溴水中萃取出来
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高一上12月月考化学试卷(解析版) 题型:推断题
A、B、C、D、E各物质的转化关系如图所示。
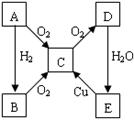
(1)当A为固体单质时,A是 (写化学式)。
①写出B的电子式: ;
②写出E与木炭反应化学方程式: 。
(2)当A为气体单质时,A是 (写化学式)。
①写出B的结构式: ;
写出下列反应的化学方程式,并回答有关问题:
②E→C: ;
③实验室制备B: 。
能不能用浓硫酸做B的干燥剂? (填“能”或“不能”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期期中考试化学试卷(解析版) 题型:填空题
常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式______________________ _。
(2)若溶液M由10mL 2 mol·L-1NaHA溶液与2mol·L-1NaOH溶液等体积混合而得,则溶液M的pH ________7 (填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为
(3)若溶液M由下列三种情况:①0.01mol·L-1的H2A溶液②0.01mol·L-1的NaHA溶液③0.02mol·L-1的HCl与0.04mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为_ _ _ _ __;pH由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是:

A.b>f
B.平衡常数K(1000℃)<K(810℃)
C.915℃、2.0MPa该反应的平衡常数为Kp=4.5MPa
D.1000℃、3.0MPa时E的转化率为83%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com