
 ,某有机物X的键线式为:
,某有机物X的键线式为:
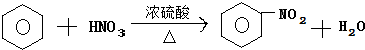 ;
; ;
;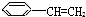 ,
,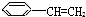 ;
; ;
; ;
;

科目:高中化学 来源: 题型:
| A、CH3-CH=CH2和CH3-CH2-CH=CH2 |
| B、CH3-CH3和CH3-CH=CH2 |
| C、CH3-CH2-CH3和CH3-CH=CH2 |
| D、CH3-CH2-CH2=CH2和CH3-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:| 温度T | T1 | T2 | T3 |
| 平衡常数K | 1.2 | 2.5 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a-3=c+2 |
| B、质子数a>b>c>d |
| C、离子的还原性Y2-<Z- |
| D、离子半径X+<W3+<Y2-<Z- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com