
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子序数由大到小的顺序是(写元素符号) 。
(2)X与Y能形成多种化合物其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系: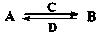 (在水溶液中进行)
(在水溶液中进行)
其中,C是溶于水显酸性的气体;D是淡黄色固体。
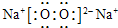
写出C的化学式 ;D的电子式 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因 ;A、B浓度均为0.1mol·L-1的混合溶液中,离子浓度由大到小的顺序是 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 。
(12分)(1)Al > Na > O > C >H(2分)(2)C2H2(1分)
(3)CO2(1分)  (1分) ①NaAlO2(1分)
(1分) ①NaAlO2(1分)
②CO32- + H2O  HCO3- + OH-(2分)
HCO3- + OH-(2分)
c(Na+) > c(HCO3-) > c(CO32-) > c(OH-) > c(H+)(2分)
NaCl、NaHCO3、CO2(或H2CO3) (2分,写不全给1分,有错的不得分)
解析试题分析:X、Y两元素最高正价与最低负价之和均为0,所以X和Y是第ⅣA族元素或第IA族元素。Z、R分别是地壳中含量最高的非金属元素和金属元素,所以Z是O,R是Al。X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,所以X是氢元素,Y是碳元素。Q与X同主族,因此Q是钠元素。
(1)五种元素原子序数由大到小的顺序是Al>Na>O>C>H。
(2)X与Y能形成多种化合物其中既含极性键又含非极性键,且相对分子质量最小的物质是乙炔,化学式是C2H2。
(3)D是淡黄色固体,所以D是过氧化钠。C是溶于水显酸性的气体,所以C应该是CO2。
①如果A、B均由三种元素组成,B为两性不溶物,所以B是氢氧化铝,则A是偏铝酸钠,其化学式为NaAlO2。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性,这说明A是碳酸钠,B是碳酸氢钠。碳酸钠溶于水水解溶液显碱性,则水解方程式是CO32- + H2O  HCO3- + OH-。溶液显碱性,且碳酸钠的水解程度大于碳酸氢钠的,所以溶液中离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)> c(H+)。溶液显中性,这说明反应中有CO2生成,所以常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有NaCl、NaHCO3、CO2(或H2CO3)。
HCO3- + OH-。溶液显碱性,且碳酸钠的水解程度大于碳酸氢钠的,所以溶液中离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)> c(H+)。溶液显中性,这说明反应中有CO2生成,所以常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有NaCl、NaHCO3、CO2(或H2CO3)。
考点:考查元素周期表的结构、化学键、电子式、溶液中离子浓度大小比较以及水解原理的有关判断和应用
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的应试能力和逻辑推理能力。该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源: 题型:
| C | D |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X的原子半径比Z的小 | B、X与Z形成的化合物只有一种 | C、Y的简单氢化物的热稳定性比Z的强 | D、R的最高价氧化物的水化物碱性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X与Y能形成多种化合物,其中既含极性键又含非极性键,其相对分子质量最小为16 | B、原子半径的顺序为:Q>R>Y>Z>X | C、X与Z、Q与Z 都可以形成原子个数比1:1和2:1的化合物 | D、化合物Q2Z2与QX,中阳离子与阴离子个数比均为1:1 |
查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷带解析) 题型:推断题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式) 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A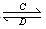 B (在水溶液中进行)
B (在水溶液中进行)
其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;由A转化为B的离子方程式为 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因: 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 。
查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷解析版) 题型:推断题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式) 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A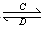 B (在水溶液中进行)
B (在水溶液中进行)
其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;由A转化为B的离子方程式为 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因: 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是 ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com