
 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
分析 X的一种氢化物分子中既有σ键又有π键,说明分子里有双键或参键,X的一种氢化物为1:2型且所有原子共平面,所以X应为碳元素,它的1:2型氢化物为乙烯;Z的L层上有2个未成对电子,即核外电子排布为1s22s22p2或1s22s22p4,X、Y、Z原子序数依次增大,所以Z为氧元素,且Y为氮元素;Q原子s能级与p能级电子数相等,则Q的核外电子排布为1s22s22p4或1s22s22p63s2,由于Q的原子序数比Z大,所以Q的电子排布为1s22s22p63s2,即Q为镁元素;而G为金属元素且原子序数介于氧和镁元素之间,所以G为钠元素;R单质是制造各种计算机、微电子产品的核心材料,R为硅元素;T处于周期表的ds区,且最外层只有一个电子,则T为Cu,据此答题.
解答 解:X的一种氢化物分子中既有σ键又有π键,说明分子里有双键或参键,X的一种氢化物为1:2型且所有原子共平面,所以X应为碳元素,它的1:2型氢化物为乙烯;Z的L层上有2个未成对电子,即核外电子排布为1s22s22p2或1s22s22p4,X、Y、Z原子序数依次增大,所以Z为氧元素,且Y为氮元素;Q原子s能级与p能级电子数相等,则Q的核外电子排布为1s22s22p4或1s22s22p63s2,由于Q的原子序数比Z大,所以Q的电子排布为1s22s22p63s2,即Q为镁元素;而G为金属元素且原子序数介于氧和镁元素之间,所以G为钠元素;R单质是制造各种计算机、微电子产品的核心材料,R为硅元素;T处于周期表的ds区,且最外层只有一个电子,则T为Cu.
(1)Y为氮元素,核外电子排布式为1s22s22p3,所以7种不同运动状态的电子,T为Cu元素,它的核外电子排布式为1s22s22p63s23p63d104s1,价电子排布为3d104s1,
故答案为:7;3d104s1;
(2)OCN-与CO2互为等电子体,所以它们结构相似,在二氧化碳中碳原子的价层电子对数为2,所以碳的杂化方式为sp杂化,则OCN-中C原子也是sp杂化,
故答案为:sp杂化;
(3)化合物甲为二氧化硅,在二氧化硅晶体中,每个硅原子周围有四个Si-O 键,所以1mol二氧化硅中含有4molSi-O 键,SiO2与HF反应的方程式为:SiO2+4HF=SiF4+2H2O,其中SiF4中硅原子的价层电子对数为4+$\frac{4-1×4}{2}$=4,没有孤电子对,所以SiF4的空间构型为正四面体,H2O中氧原子的价层电子对数为2+$\frac{6-1×2}{2}$=4,有2对孤电子对,所以H2O的空间构型为V形,
故答案为:4;正四面体形、V形;
(4)在NaF、MgF2、SiF4中NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高,
故答案为:NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高;
(5)向硫酸铜溶液中逐滴加入氨水至过量,开始生成氢氧化铜沉淀,后来沉淀溶解生成四氨合铜离子,其反应的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-,
故答案为:Cu2++2 NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
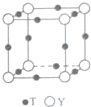
(6)与Y离子最近的T离子处于棱上且故Y离子对称,故Y离子配位数为6;
晶胞中N原子数目为8×$\frac{1}{8}$=1,Cu原子数目为12×$\frac{1}{4}$=3,则晶胞质量为$\frac{14+64×3}{{N}_{A}}$g,晶胞体积为(a cm)3,则:(a cm)3×bg•cm-3=$\frac{14+64×3}{{N}_{A}}$g,整理得NA=$\frac{206}{b{a}^{3}}$,
故答案为:6;$\frac{206}{b{a}^{3}}$.
点评 本题是对物质结构的考查,涉及核外电子的排布及运动状态、等电子体、分子构型、晶体类型与性质、配合物、晶胞计算等,注意理解均摊法有关晶胞计算,题目难度中等.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm互为同素异形体 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm具有相同核外电子排布 | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的性质完全相同 | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质子数不同,但中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 操作 | 现象 | 结论 |
| A | 向FeSO4溶液中滴入少量酸性KMnO4溶液 | KMnO4溶液紫色褪去 | Fe2+有氧化性 |
| B | 向Na2SiO3溶液中通入适量的CO2 | 产生白色胶状物质 | 酸性:H2CO3>H2SiO3 |
| C | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液呈橙红色 | 氧化性:Cl2>Br2 |
| D | 向Al2(SO4)3溶液中滴加过量氨水 | 溶液先浑浊后澄清 | Al3+与NH3•H2O不能大量共存 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3只发生氧化反应 | B. | 反应消耗12g C时电子转移5mol | ||
| C. | 还原产物只有K2S和 N2 | D. | 被氧化与被还原的S为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池不宜在高温下工作 | |
| B. | 若该电池为酸性介质,正极反应式为:O2+4e-+4H+═2H2O | |
| C. | 放电过程中,电池内阳离子向正极迁移 | |
| D. | 若该电池为碱性介质,以葡萄糖为原料并完全氧化,负极反应式为:C6H12O6-24e-+6H2O═6CO2↑+24H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32g O2和16g O3的混合物中,含有O原子数目为2NA | |
| B. | 标准状况下,1mol Na2O 和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1mol NaHSO4溶于水或受热熔化,电离出来的离子数目均为2NA | |
| D. | 在K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O中,若生成71g Cl2,转移的电子数目为 $\frac{2}{3}$NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用LED照明灯属于“低碳生活”方式 | |
| B. | 在家用电热水器不锈钢内胆镶嵌镁棒,以防止内胆被侵蚀 | |
| C. | 施用适量石灰乳可降低盐碱地(含较多NaCl,Na2CO3) | |
| D. | 研制高性能的耐磨轮胎,可减少细颗粒物(PM2.5)的产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com