
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料)。
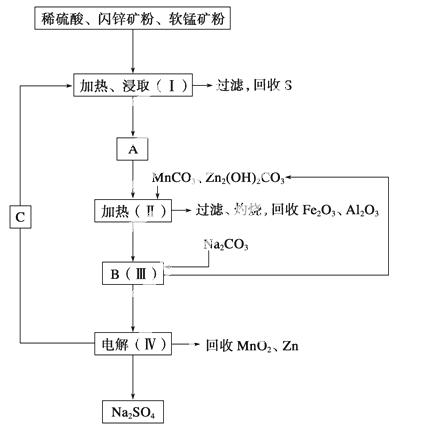
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②Ⅳ中电解方程式为MnSO4+ZnSO4+2H2OMnO2+Zn+2H2SO4。
(1)A中属于还原产物的是______ ____。
____。
(2)加入MnCO3、Zn2(OH)2CO3的作用是_____________________________________
________________________________________________________________________。
Ⅱ需要加热的原因是____________________________________________________。
C的化学式是________________________。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是________。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是________。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进行的操作有蒸发浓缩、________、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是________。
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是
A.生成42.0LN2(标准状况)
B.有0.250molKNO3被氧化
C.转移电子的物质的量为1.25mol
D.被氧化的N原子的物质的量为3.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图
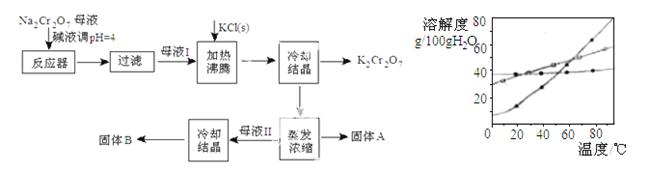 (1)由Na2Cr2O7生产K2Cr2O7的化学方程式为
(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为  。通过冷过结晶析出大量K2Cr2O7的原因是 。
。通过冷过结晶析出大量K2Cr2O7的原因是 。
(2)向Na2Cr2O7母液中加碱液调pH的目的是 。
(3)固体A主要为 (填化学 式)
式) ,固体B主要为 (填化学式)。
,固体B主要为 (填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液 (填“I”“II”或“III”)中,既能提高产率又可使能耗最低。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国科学家理查德·海克和日本科学家根岸英一、铃木彰因在研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂,长期使用催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收。一种由废催化剂制取氯化钯的工艺流程如下:
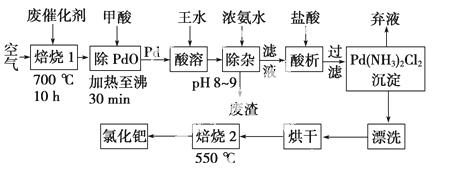
(1)废钯催化剂经烘干后,再在700 ℃的高温下焙烧,焙烧过程中需通入足量空气的原因是________________________________________________________________________;
甲酸还原氧化钯的化学方程式为____________________ ______________________。
______________________。
(2)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为______________________。
(3)钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如下图1~图3所示,则王水溶解钯精渣的适宜条件(温度、时间和王水用量)为__________、__________、__________。
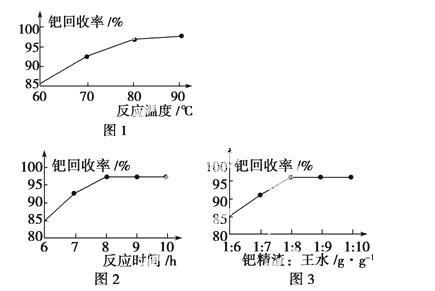
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)2]2+,此时铁的存在形式是________________________________________________________________________(写化学式)。
(5)700 ℃焙烧1的目的是________________;550 ℃焙烧2的目的是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业、硫酸工业的生产工艺 流程如图所示 。
。
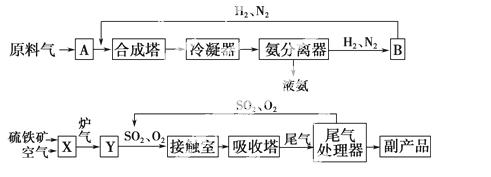
合成塔和接触室中的反应分别为
N2(g)+3H2(g) 2NH3(g) ΔH<0;
2SO2(g)+O2(g) 2SO3(g) ΔH<0。
(1)写出流程中设备的名称:B________,X________。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是___________________。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是________(填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是_______________。
(5)工业生产中常用氨-酸法进行尾气脱硫,以达到消 除污染、
除污染、 废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
(6)根据化学 平衡移动原理,下列条件或措施合理的是________(填序号)。
平衡移动原理,下列条件或措施合理的是________(填序号)。
①合成氨工业在高压下进行
②合成氨工业和硫酸工业都使用催化剂
③及时将氨液化而分离
④硫酸工业中,净化后的炉气中要有过量空气
⑤合成氨工业和硫酸工业都采用适宜的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
右图模 拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是
拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是

A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)①BF3与一定量的水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
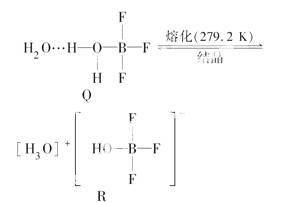
晶体Q中各种微粒间的作用力不涉及________(填序号)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
②已知苯酚具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子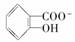 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是__________________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________Ka(苯酚)(填“>”或“<”),其原因是__________________。
(2)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/ (kJ·mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是______________________。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在P+CuSO4+H2O—→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com