
| A. | [AgCl2]- | B. | [Ag(NH3)2]+ | C. | [Ag(S2O3)2]3- | D. | [Ag(CN)2]- |
分析 配合物也叫络合物,为一类具有特征化学结构的化合物,由中心原子或离子(统称中心原子)和围绕它的称为配位体(简称配体)的分子或离子,完全或部分由配位键结合形成,配合物中中心原子提供空轨道,配体提供孤电子对.
配离子中最稳定的离子规律:配合物中中心离子正电荷相同、半径越小、离子势越大,越稳定;配位原子电负性大,吸引电子能力强,则给出电子对和中心元素配合能力越弱,配体对分裂能越大,配离子越稳定,配体对分裂能大小由弱至强的顺序是:I-<Br-<S2-<S2O32-<SCN-<Cl-<NO3-<F-<OH-<C2O42-<H2O<NCS-<NH3<en(乙二胺)<bipy(联吡啶)<NO2-<CN-<CO,据此分析解答.
解答 解:[AgCl2]-、[Ag(NH3)2]+、[Ag(S2O3)2]3-、[Ag(CN)2]-中心离子都是Ag+离子,配体对分裂能越大,配离子越稳定,配体对分裂能大小由弱至强的顺序是:I-<Br-<S2-<S2O32-<SCN-<Cl-<NO3-<F-<OH-<C2O42-<H2O<NCS-<NH3<en(乙二胺)<bipy(联吡啶)<NO2-<CN-<CO,所以配体对分裂能大小由弱至强的顺序是:Cl-<S2O32-<NH3<CN-,配体CN-的分裂能更大,其稳定性越大,
故选D.
点评 本题考查配合离子的性质,掌握配离子中稳定的离子比较规律是解答关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 质量数为118 | B. | 中子数为179 | C. | 质子数为118 | D. | 电子数为118 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
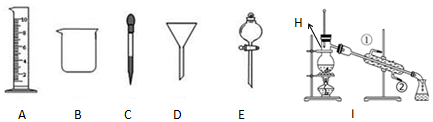
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
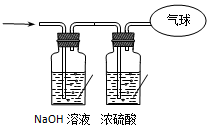 现有16.4克O2和CO2的混合气体,在标准状况下其体积为8.96L.请回答下列问题:
现有16.4克O2和CO2的混合气体,在标准状况下其体积为8.96L.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶未经干燥不能用来配制溶液 | |
| B. | 用铁坩埚灼烧烧碱 | |
| C. | 中和热的测定实验中用环形玻璃棒搅拌 | |
| D. | 加热蒸发皿时不用石棉网 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L的CCl4中含CCl4分子数为NA | |
| B. | 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 | |
| C. | 0.1 mo1•L-1 MgCl2溶液中含Cl-数为0.2NA | |
| D. | 3.9 g Na2O2晶体中含有的离子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成相差一个或若干个CH2原子团的有机物是同系物 | |
| B. | 乙酸的官能团是羧基,乙醇的官能团是羟基 | |
| C. | 乙烯的产量通常用来衡量一个国家的石油化工发展水平 | |
| D. | 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com