把4mol A和4mol B混合放入容积为2L的密闭容器里,发生反应3A(g)+2B(g)═x C(g)+2D(g),经5s后反应达平衡.在此5s内C的平均反应速率为0.1mol?L-1?s-1,同时生成2mol D.试计算:
(1)达到平衡状态时B的转化率;
(2)试算x的值;
(3)若温度和压强维持不变,当生成2mol D时,此时容器内气体的体积是多少?
【答案】
分析:(1)结合方程式3A(g)+2B(g)═x C(g)+2D(g),利用平衡三部曲求出各物质的物质的量,再利用转化率定义计算;
(2)结合方程式3A(g)+2B(g)═x C(g)+2D(g),利用平衡三部曲求出各物质的物质的量,求出x的值;
(3)根据温度和压强维持不变,物质的量和体积成正比;
解答:解:生成C的物质的量为0.1mol?L
-1?s
-1×5s×2L=1mol,
(1)3A(g)+2B(g)═x C(g)+2D(g),
起始(mol) 4 4 0 0
反应(mol) 3 2 1 2
平衡(mol) 1 2 1 2
故平衡状态时B的转化率
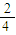
×100%=50%;
(2)3A(g)+2B(g)═x C(g)+2D(g),
起始(mol) 4 4 0 0
反应(mol) 3 2 1 2
平衡(mol) 1 2 1 2
因反应的物质的量之比等于化学计量数之比,故x=1;
(3)反应前气体的总物质的量为8mol,体积为2L,反应后气体的总物质的量为1+2+1+2=6mol,因据温度和压强维持不变,物质的量和体积成正比,故容器内气体的体积是1.5L.
点评:考查化学平衡的有关计算,难度不大,注意平衡三部曲应用.

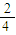 ×100%=50%;
×100%=50%;
