
 在恒容密闭容器中通入X并发生反应:2X(g)?Y(g),在温度T1、T2下,Y的物质的量浓度c(Y)随时间t变化的曲线如图所示,下列叙述正确的是( )
在恒容密闭容器中通入X并发生反应:2X(g)?Y(g),在温度T1、T2下,Y的物质的量浓度c(Y)随时间t变化的曲线如图所示,下列叙述正确的是( )| A. | 该反应进行到M点放出的热量大于进行到W点放出的热量 | |
| B. | N点的逆反应速率v逆大于W点的逆反应速率v逆 | |
| C. | T1>T2 | |
| D. | M点时再加入一定量X,平衡后X的转化率减小 |
分析 由温度T1、T2下,Y的物质的量浓度c(Y)随时间t变化的曲线图可知,T2先达到平衡,则T2>T1,可知升高温度c(Y)减小,则升高温度平衡逆向移动,该反应为放热反应,
A.M、W均为平衡点,M点时平衡正向移动程度大;
B.温度越高时反应速率越大;
C.T2先达到平衡;
D.M点时再加入一定量X,压强增大,平衡正向移动.
解答 解:由温度T1、T2下,Y的物质的量浓度c(Y)随时间t变化的曲线图可知,T2先达到平衡,则T2>T1,可知升高温度c(Y)减小,则升高温度平衡逆向移动,该反应为放热反应,
A.M、W均为平衡点,M点时平衡正向移动程度大,正反应为放热反应,则该反应进行到M点放出的热量大于进行到W点放出的热量,故A正确;
B.T2>T1,则N点的逆反应速率v逆小于W点的逆反应速率v逆,故B错误;
C.T2先达到平衡,则T2>T1,故C错误;
D.M点时再加入一定量X,压强增大,平衡正向移动,平衡后X的转化率增大,故D错误;
故选A.
点评 本题考查物质的量浓度随时间变化曲线,为高频考点,把握温度对平衡及反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 在硫酸氢钾溶液中加入Ba(OH)2溶液至沉淀完全时:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 工业上用三氯化铁溶液腐蚀印刷电路板:2Fe3++3Cu═3Cu2++2Fe | |
| C. | 碘化钾溶液酸化后滴入少量双氧水:2I-+H2O2═I2+2OH- | |
| D. | 向次氯酸钠溶液中通人少量SO2:2ClO-+SO2+H2O═2HClO+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用图所示装置除去Cl2中含有的HCl | |
| B. | 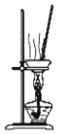 用图所示装置蒸干MgCl2饱和溶液制备MgCl2•6H2O晶体 | |
| C. |  用环己烷萃取碘水时将两者混合后需如图3所示用力振荡 | |
| D. |  继续煮沸图所示溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述II | 判断 |
| A | 碳酸钠溶液可用于治疗胃病 | Na2CO3可与盐酸反应 | I对,II对,有 |
| B | 盛放氢氧化钠溶液的试剂瓶用橡胶塞 | 氢氧化钠可以与玻璃中的二氧化硅反应生成粘性的硅酸钠 | I错,II 对,有 |
| C | 铝制品很耐腐蚀 | 铝在常温下很难被氧气氧化 | I对,II对,有 |
| D | 向漂白粉溶液中滴入少量白醋以增强漂白能力 | 醋酸的酸性比次氯酸强 | I对,II对,有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 甲烷与Cl2反应 油脂的皂化 | 均为取代反应 |
| B | 苯滴加到溴水中,溴水褪色,乙烯通入到溴水中,溴水褪色 | 均发生了加成反应 |
| C | Cl2+2Br?=2Cl?+Br2 CO+CuO=Cu+CO2 | 均为置换反应 |
| D | SO2+H2O=H2SO3 2F2+2H2O=4HF+O2 | 均为水作还原剂的氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用液溴和苯在催化剂作用下制溴苯: +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$ +HBr +HBr | |
| B. | 苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 向氯乙烷水溶液中加入氢氧化钠溶液共热:CH3CH2Cl+NaOH$\stackrel{△}{→}$CH2=CH2+NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 氢氧燃料电池可以使用在航天飞机上,图为其反应原理示意图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,图为其反应原理示意图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该电池的a、b极材料可以是同种金属 | |
| B. | 该电池是一种高效、环境友好的发电装置 | |
| C. | 外电路中电子由电极b通过导线流向电极a | |
| D. | 该电池的总反应:2H2+O2═2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com