
| 改变的条件 | 水的电离程度 | c(H+) | pH | 酸碱性 | c(H+)?c(OH-) |
| ①通入CO2气体 | |||||
| ②通入NH3气体 | |||||
| ③通入HCl气体 | |||||
| ④加入NaOH固体 | | ||||
| ⑤加热 |
| 改变的条件 | 水的电离程度 | c(H+) | pH | 酸碱性 | c(H+)?c(OH-) |
| ①通入CO2气体 | 减小 | 增大 | 减小 | 酸性 | 不变 |
| ②通入NH3气体 | 减小 | 减小 | 增大 | 碱性 | 不变 |
| ③通入HCl气体 | 减小 | 增大 | 减小 | 酸性 | 不变 |
| ④加入NaOH固体 | 减小 | 减小 | 增大 | 碱性 | 不变 |
| ⑤加热 | 增大 | 增大 | 减小 | 中性 | 增大 |


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
| A、久置的氯水与新制的氯水,都能使有色布条褪色 |
| B、氯气、液氯和氯水是同一种物质 |
| C、碘化钾溶液中加淀粉溶液变蓝色 |
| D、加碘盐就是在食盐中加入适量的碘酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 和
和
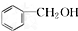 和
和
 和
和


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、混合气体的相对分子质量 |
| D、C的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应中氧化剂是氧气 |
| B、铜是导电性最好的金属 |
| C、可以将铜的冶炼和硫酸的生产联合在一起 |
| D、在Cu2S中铜的化合价为+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉和纤维素化学式均为(C6H10O5)n,但不互为同分异构体 |
| B、摄入人体的纤维素在酶的作用下能水解为葡萄糖 |
| C、糖类、蛋白质、油脂都属于天然高分子化合物 |
| D、所有糖类物质都有甜味,但不一定都溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 与足量的NaOH溶液混合,在一定条件下反应,则NaOH的物质的量共消耗了( )
与足量的NaOH溶液混合,在一定条件下反应,则NaOH的物质的量共消耗了( )| A、8 mol |
| B、6 mol |
| C、5 mol |
| D、4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用滤纸称量氢氧化钠固体 |
| B、溶解后未冷却直接定容 |
| C、容量瓶不干燥,存有少量蒸馏水 |
| D、胶头滴管加水定容时仰视刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com