
| A. | 煤经过分馏可得到焦炉气、煤焦油和焦炭 | |
| B. | 甲烷、汽油、酒精都是碳氢化合物,都可作燃料 | |
| C. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| D. | 蛋白质、淀粉、油脂均能发生水解反应 |
分析 A、煤经过干馏可得焦炉气、煤焦油和焦炭;
B、仅由碳和氢两种元素组成的有机化合物称为碳氢化合物;
C、聚乙烯中无碳碳双键;
D、蛋白质水解为氨基酸,淀粉水解为葡萄糖,油脂水解为甘油和高级脂肪酸.
解答 解:A、煤经过干馏可得焦炉气、煤焦油和焦炭,煤无分馏,故A错误;
B、酒精含有碳氢氧元素,不属于碳氢化合物,故B错误;
C、聚乙烯中无碳碳双键,故不能和溴的四氯化碳发生加成反应,不能使溴的四氯化碳褪色,故C错误;
D、蛋白质水解为氨基酸,淀粉水解为葡萄糖,油脂水解为甘油和高级脂肪酸,即三者均能水解,故D正确.
故选D.
点评 本题考查化学的应用,难度不大,注意蛋白质、淀粉和油脂均能水解.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 在SiO2晶体中,由Si、O构成的最小单元环中共有8个原子 | |
| B. | 在28g晶体硅中,含Si-Si共价键个数为4NA | |
| C. | 金刚石的熔沸点高于晶体硅,是因为C-C键键能小于Si-Si键 | |
| D. | 镁型和铜型金属晶体的配位数均为12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中滴加足量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 铜片与浓HNO3:Cu+2NO3-+2H+=Cu2++2NO2↑+H2O | |
| C. | NH4HCO3溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 一水合氨的电离:NH3•H2O=NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,2,4-三甲基-1-丁醇 | D. | 2,3-二乙基-1-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | |
| B. | 加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+$\frac{1}{2}$c(SO32-) | |
| C. | 加入少量NaOH溶液,$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$、$\frac{c(O{H}^{-})}{c({H}^{+})}$的值均增大 | |
| D. | 加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
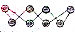 )所示,该单质与NaOH溶液反应时产物之一为Na2SO3,写出该反应的离子方程式:3S8+48OH-=16S2-+8SO32-+24H2O.
)所示,该单质与NaOH溶液反应时产物之一为Na2SO3,写出该反应的离子方程式:3S8+48OH-=16S2-+8SO32-+24H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 最外层电子数 | 次外层电子数 |
| D | x | x+4 |
| E | x+1 | x+4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com