
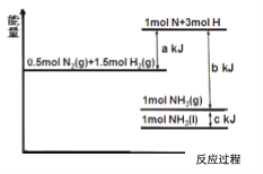
【题目】I、根据能量变化示意图,请写出氮气和氢气合成液态 的氨气的热化学方程式_____;
Ⅱ、已知:NO2(g)+ SO2(g)![]() SO3(l)+ NO(g)ΔH=-51.5kJ·mol-1
SO3(l)+ NO(g)ΔH=-51.5kJ·mol-1
若在一定条件下,将 NO2 与 SO2 以体积比 1:2 置于恒容密闭容器 中发生上述反应,
①下列能说明反应达到平衡状态的是_____。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3 和 NO 的物质的量之比保持不变 d.每消耗 1 mol SO3 的同时生成 1 molNO2
e.容器内气体密度不变
②恒容密闭容器中发生上述反应时,若加入 Ar 气,反 应速率_____(变大、变小或不变)。
【答案】 N2(g)+3H2(g)![]() 2NH3(l)ΔH=2(a-b-c)kJ·molˉ1 abe 不变
2NH3(l)ΔH=2(a-b-c)kJ·molˉ1 abe 不变
【解析】试题分析:I、反应的焓变=生成物的总能量-反应物的总能量;Ⅱ、①根据平衡标志分析;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变;
解析:I、反应的焓变=生成物的总能量-反应物的总能量;氮气和氢气合成液态的氨气的热化学方程式N2(g)+3H2(g) ![]() 2NH3(l) ΔH=2(a-b-c)kJ·molˉ1;Ⅱ、①a.根据方程式,反应前后气体物质的量改变,所以压强是变量,体系压强保持不变一定平衡,故a正确; b.混合气体颜色保持不变,说明NO2浓度不变,一定达到平衡状态,故b正确; c.反应过程中SO3 和 NO 的物质的量之比始终是1:1,所以SO3 和 NO 的物质的量之比保持不变不一定达到平衡状态,故c错误; d.每消耗 1 mol SO3 的同时生成 1 molNO2,都是指逆反应,故d不一定平衡,d错误; e.根据
2NH3(l) ΔH=2(a-b-c)kJ·molˉ1;Ⅱ、①a.根据方程式,反应前后气体物质的量改变,所以压强是变量,体系压强保持不变一定平衡,故a正确; b.混合气体颜色保持不变,说明NO2浓度不变,一定达到平衡状态,故b正确; c.反应过程中SO3 和 NO 的物质的量之比始终是1:1,所以SO3 和 NO 的物质的量之比保持不变不一定达到平衡状态,故c错误; d.每消耗 1 mol SO3 的同时生成 1 molNO2,都是指逆反应,故d不一定平衡,d错误; e.根据![]() ,气体质量是变量,体积是恒量,所以密度是变量,容器内气体密度不变一定达到平衡状态,故e正确;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变,所以反应速率不变。
,气体质量是变量,体积是恒量,所以密度是变量,容器内气体密度不变一定达到平衡状态,故e正确;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变,所以反应速率不变。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,救了数千万人的生命,青蒿素分子结构如图.下列有关说法正确的是( ) 
A.青蒿素可溶于乙醚和水
B.青蒿素的晶体为分子晶体,化学式为C16H20O5
C.青蒿素与NaOH溶液不反应
D.青蒿素含有过氧键,一定条件下有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的同周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物对应水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号: A ___,B____,C____,D____,E________。
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式:_____________________________。
(3)比较C、D的最高价氧化物对应水化物的酸性:_____________(用化学式表示) 。
(4)用离子方程式表示实验室制取E的单质的原理:____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组利用如图装置进行某些气体的制备和性质实验,图中加持装置有省略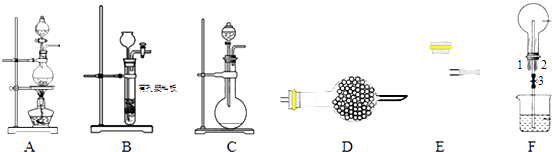
(1)为制取干燥氨气,可将装置C与装置D连接,则装置D中 的固体宜选用a.碱石灰 b.无水氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净干燥的氯气,则两个E装置内的药品依次是
(3)装置F可用于探究氯气和氨气反应,实验室打开开关1、3,关闭2,先向烧瓶中通入 , 然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体.实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子 .
(4)利用装置A、E,可设计实验比较氯离子和溴离子的还原性强弱,能证明结论的实验现象是 . 若利用装置A、E进行乙烯与溴水反应的实验,必须对装置A进行的改动是 .
(5)将装置B、C分别于F相连后,进行硫化氢和二氧化硫反应的实验,烧杯中的试剂所起的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“水煤气(CO、H2)﹣空气”燃料电池的工作原理如图所示,其中a、b均
为惰性电极.下列叙述正确的是( )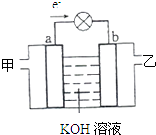
A.甲处通入的是空气,乙处通入的是水煤气
B.a电极发生还原反应,b电极发生氧化反应
C.用该电池电镀铜,若待镀金属增重6.4g,至少消耗标准状况下的水煤气2.24L
D.a电极的反应式包括:CO+4OH﹣+2e﹣═CO32﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是( ) 
A.溶液pH≤2时,生铁发生析氢腐蚀
B.在酸性溶液中生铁可能发生吸氧腐蚀
C.析氢腐蚀和吸氧腐蚀的速率一样快
D.两溶液中负极反应均为:Fe﹣2e﹣═Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不用其它任何试剂鉴别下列5种物质的溶液:①KOH ②MgSO4 ③Ba(NO3)2 ④CuCl2 ⑤KNO3,被鉴别出来的正确顺序是
A. ⑤④③②① B. ④①②③⑤ C. ②③①④⑤ D. ④①⑤②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知,Fe2+结合S2﹣的能力大于结合OH﹣的能力,而Al3+则正好相反.在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
A.Al2S3、FeS和S
B.Fe(OH)3和Al(OH)3
C.Fe2S3和Al(OH)3
D.FeS、Al(OH)3和S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com