绿矾(FeSO
4?7H
2O)是治疗缺铁性贫血的特效药.某学校的化学兴趣小组的同学对绿矾进行了如下的探究:
(一)FeSO
4?7H
2O的制备
该化学兴趣小组的同学在实验室通过如下实验由废铁屑(含少量氧化铜、氧化铁等杂质)制备FeSO
4?7H
2O晶体:
①将5% Na
2CO
3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na
2CO
3溶液,然后将废铁屑用水洗涤2~3遍.
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO
4?7H
2O晶体放在一个小广口瓶中,密闭保存.
请回答下列问题:
(1)实验步骤①的目的是
.
(2)实验步骤②明显不合理,理由是
.
(3)为了洗涤除去晶体表面附着的硫酸等杂质,实验步骤④中用少量冰水洗涤晶体,原因是
.
(二)探究绿矾(FeSO
4?7H
2O)热分解的产物
已知SO
3的熔点是16.8℃,沸点是44.8℃,该小组设计如图所示的实验装置(图中加热、夹持仪器等均省略):
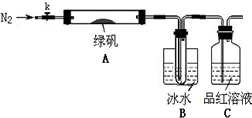
实验过程:
①仪器连接后,检查装置A与B气密性;
②取一定量绿矾固体置于A中,通入N
2以驱尽装置内的空气,关闭k,用酒精灯加热硬质玻璃管;
③观察到A 中固体逐渐变红棕色,B中试管收集到无色液体,C中溶液褪色;
④待A中反应完全并冷却至室温后,取少量反应后固体于试管中,加入硫酸溶解,取少量滴入几滴KSCN溶液,溶液变红色;
⑤往B装置的试管中滴入几滴BaCl
2溶液,溶液变浑浊.
(4)实验结果分析
结论1:B中收集到的液体是
;
结论2:C中溶液褪色,可推知产物中有
;
结论3:综合分析上述实验③和④可推知固体产物一定有Fe
2O
3.
实验反思:
(5)请指出该小组设计的实验装置的明显不足:
.
(6)分解后的固体中可能含有少量FeO,取上述实验④中盐酸溶解后的溶液少许于试管中,选用一种试剂鉴别,该试剂最合适的是
.
a.氯水和KSCN溶液 b.酸性KMnO
4溶液 c.H
2O
2 d.NaOH溶液.

