
| A. | H、D、T互为同素异形体 | B. | 中子数为20的氯原子: | ||
| C. | 四氯化碳的电子式: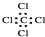 | D. | Cl-的结构示意图: |
分析 A.同素异形体是指同种元素组成的不同单质;
B.原子符号中左上角标注的是质量数,质量数=质子数+中子数;
C.四氯化碳的电子式中,氯原子的最外层达到8电子稳定结构,漏掉了氯原子的最外层3对未成键电子;
D.氯原子核电荷数为17,得到一个电子形成氯离子,据此画出离子结构示意图.
解答 解:A.H、D、T是氢元素的不同原子互为同位素,不是同素异形体,故A错误;
B.中子数为20的氯原子,氯元素的质子数为17,中子数为20的氯原子的质量数为37,该原子正确的表示方法为:1737Cl,故B错误;
C.四氯化碳分子中含有4个碳氯键,碳原子和氯原子最外层达到8电子稳定结构,四氯化碳正确的电子式为: ,故C错误;
,故C错误;
D.Cl-的质子数为17,电子数为18,Cl-结构示意图为: ,故D正确;
,故D正确;
故选D.
点评 本题考查同位素、同素异形体、电子式书写、离子结构示意图的书写,题目难度不大,熟悉概念实质是解题的关键.


科目:高中化学 来源: 题型:解答题
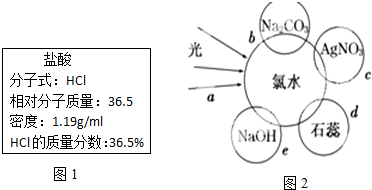
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
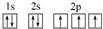 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.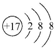 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
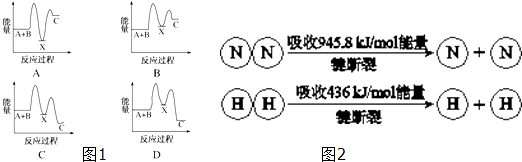
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
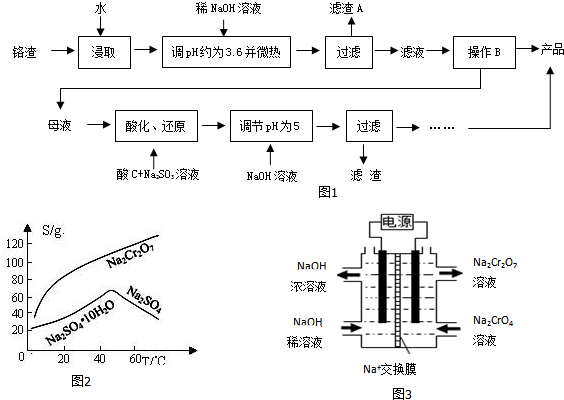
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
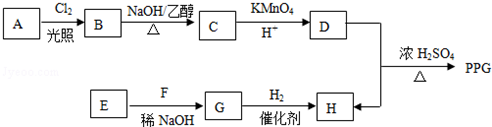
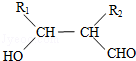
 .
. .
. .
. (写构简式)
(写构简式)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com