
某溶液中含有Fe2+、Al3+、Ag+、Cu2+,为了分别得到各含一种金属阳离子的沉淀,可采取:①通入H2S;②通入CO2;③加HCl溶液;④加NaOH溶液4个步骤,设试剂均过量,且每次都把所生成的沉淀过滤出来。其正确的操作顺序是 ( )
A.③①④② B.①③④②
C.④② ①③ D.④②③①
①③ D.④②③①
科目:高中化学 来源: 题型:
锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造如图a所示。
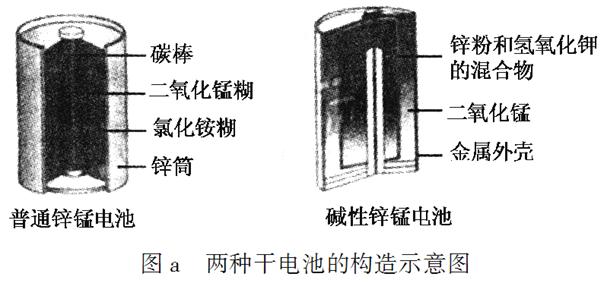
回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:
Zn+2NH4Cl+2MnO2===Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是________,电解质的主要成分是________,正极发生的主要反应是________________________________。
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是__________________________________________________________。
(2)图b表示回收利用废旧普通锌锰电池的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。

①图b中产物的化学式分别为A________,B________。
②操作a中得到熔块的主要成分是K2MnO4。操作b中,绿色的K2MnO4溶液反应后生成紫色溶液和一种黑褐色固体,该反应的离子方程式为________________________________________。
③采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五瓶无标签的溶液,它们可能是NH4Cl、Na2SO4、BaCl2、AgNO3、HNO3五种溶液,为鉴别它们进行了如下实验。
①将A分别滴加到B、C、D、E四种溶液中,则可以确定A;
②将B分别滴加到C、D、E三种溶液中,则可确定B;
③将C分别滴加到D、E两种溶液中,则可确定C;
④将氢氧化钡溶液滴入E中,没有明显实验现象,则可以确定E。
回答下列问题:
(1)A不可能是AgNO3,判断的依据是________。
(2)A、B、C、D、E的化学式分别为:A ,B_______,C ,D ,E 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是( )
A.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液
B.将NH4Cl溶液蒸干制备NH4Cl固体
C.用萃取分液的方法除去酒精中的水
D.用可见光束照射以区别溶液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组实验:①除去混在植物油中的水;②回收碘的CCl4溶液中的CCl4;③用食用酒精浸泡中草药提取其中的有效成分。以上实验采用的正确方法依次是 ( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。盐体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO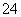 、Cl-等)来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
、Cl-等)来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
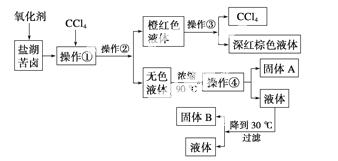
请根据以上流程,回答相关问题:
(1)操作①是________;操作②是________;操作③是_________________________;
操作④所需要的玻璃仪器有________________________________________________。
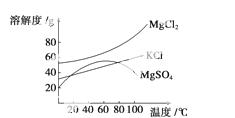
(2)参照如图所示溶解度曲线,欲得到较纯净的氯化钾晶体需用少量的________(填“热水”或“冷水”)洗涤固体_________________________________________________
(填“A”或“B”)。
(3)在实验室常用减压的方法进行过滤,俗称抽滤,试猜想这种过滤方法的优点是
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在甲苯中,加入少量酸性高锰酸钾溶液,振荡后溶液褪色 ,下列解释正确的是 ( )
,下列解释正确的是 ( )
A.甲基受苯环的影响而易被氧化
B.苯环被KMnO4所氧化而破坏
C.甲苯中碳原子数比苯分子中原子数多
D.苯环和侧链相互影响,同时被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)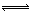 2NH3(g) ∆H=—92.4kJ•mol‾1
2NH3(g) ∆H=—92.4kJ•mol‾1
一种工业合成氨的简易流程图如下:
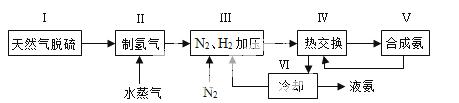
(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式: 。
(2)步骤II中制氯气原理如下:
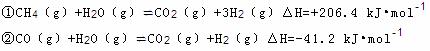
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 。
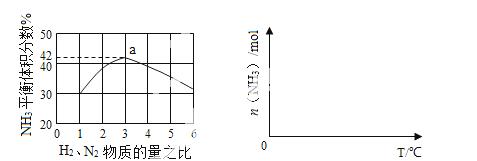
(3)下左图表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据 图中a点数据计算N2的平衡体积分数: 。
图中a点数据计算N2的平衡体积分数: 。
(4)依据温度对合成氨反应的影响,在下右图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号) ,简述本流程中提高合成氨原料总转化率的方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是( )
A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com