
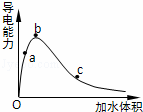
一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )
|
| A. | a、b、c三点溶液的pH:c<a<b |
|
| B. | a、b、c三点醋酸的电离程度:a<b<c |
|
| C. | 若用湿润的pH试纸测量a处溶液的pH,测量结果偏小 |
|
| D. | a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b |
考点:
弱电解质在水溶液中的电离平衡;电解质溶液的导电性.
专题:
电离平衡与溶液的pH专题.
分析:
A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
B.随水的增多,醋酸的电离程度在增大;
C.用湿润的pH试纸测量酸性的pH,溶液稀释;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同.
解答:
解:A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,故A错误;
B.随水的增多,醋酸的电离程度在增大,所以a、b、c三点醋酸的电离程度:a<b<c,故B正确;
C.用湿润的pH试纸测量酸性的pH,溶液稀释,pH增大,故C错误;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同,所以a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:a=b=c,故D错误;
故选B.
点评:
本题考查电解质的电离,题目难度中等,本题注意分析图象,把握弱电解质的电离特征,易错点为C,注意氢离子浓度越大,其溶液的pH越小.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
下列情况可能引起水污染的是( )
①城市污水的任意排放 ②农业生产中农药、化肥使用不当 ③海上石油泄漏 ④工业生产中废液、废气、废渣任意排放.
|
| A. | 只有①③ | B. | 只有①④ | C. | 只有②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分别取pH均等于2的盐酸和醋酸各l00mL,稀释2倍后,再分别加入足量锌粉,在相同条件下充分反应,下列有关叙述正确的是
( )
|
| A. | 反应开始时,盐酸和醋酸分别与锌反应的速率一样大 |
|
| B. | 反应开始时,盐酸与锌反应的速率大 |
|
| C. | 盐酸和醋酸分别与锌反应放出的氢气一样多 |
|
| D. | 醋酸与锌反应放出氢气多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在不同情况下测得A(g)+3B(g)⇌2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
|
| A. | υ(D)=0.4 mol•L﹣1•s﹣1 | B. | υ(C)=0.5 mol•L﹣1•s﹣1 |
|
| C. | υ(B)=0.6 mol•L﹣1•s﹣1 | D. | υ(A)=2 mol•L﹣1•min﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在指定的环境中可能大量共存的是( )
|
| A. | 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+ |
|
| B. | 滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl﹣、NO3﹣ |
|
| C. | 与金属铝反应只能放出氢气的溶液:NO3﹣、K+、Cl﹣、Na+、OH﹣ |
|
| D. | c(H+)>c(OH﹣)的溶液中:Na+、K+、SO42﹣、S2﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃和200kPa的条件下,反应aA(g)⇌bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步压缩体系的体积,增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度.
| 压强(kPa) | 200 | 500 | 1000 |
| B的浓度(mol/L) | 0.04 | 0.1 | 0.27 |
根据表中的数据,回答下列问题:
(1)压强从200kPa增加到500kPa时,平衡 移动(填“正向”或“逆向”或“不”),理由是 .
(2)压强从500kPa增加到1000kPa时,平衡 移动(填“正向”或“逆向”或“不”),其原因可能为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中:①石灰水 ②Na2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是()
A. ②④⑤ B. ①② C. ①②⑤ D. 只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
以下是依据一定的分类标准,对某些物质与水的反应情况进行分类的分类图.请根据你所学的知识按要求填空:
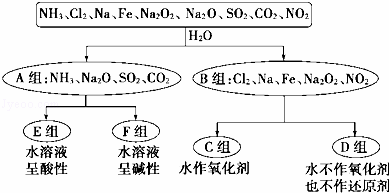
(1)上述第一级分类标准(分成A、B组的依据)是:
(2)D组物质包括 (填化学式).
(3)C组物质中某一物质在常温时能与冷水反应,其化学方程式为 .
(4)D组中某一物质与E组中某一物质在水中反应生成两种强酸,写出该反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下的密闭容器中,可逆反应A(g)+3B(g)2C(g)(g表示气态),在下列四种状态中处于平衡状态的是( )
| 速率 | A | B | C | D |
| v正/mol·(L·s)-1 | vA=1 | vB=2 | vA=1 | vC=1 |
| v逆/mol·(L·s)-1 | vB=1 | vC=2 | vC=2 | vC=2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com