
【题目】已知:2NO(g)![]() N2(g)+O2(g) △H=-181.5 kJ/mol。某科研小组尝试利用固体表面催化工艺进行NO的分解。若用
N2(g)+O2(g) △H=-181.5 kJ/mol。某科研小组尝试利用固体表面催化工艺进行NO的分解。若用![]() 、
、![]() 、
、![]() 和
和![]() 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是
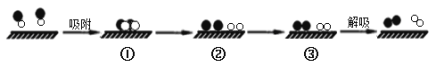
A.①B.②C.③D.无法确定
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中X、Y、Z三种气体物质的量随时间的变化关系曲线如图所示。
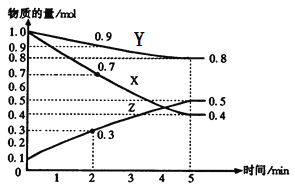
(1)由图中的数据分析,该反应的化学方程式为_____________________。
(2)反应开始至5min,Z的平均反应速率为__________;
(3)反应开始至5min,正反应速率逐渐______;(填“增大”“减小”)逆反应速率逐渐______,(填“增大”“减小”)5min后Z的物质的量不再改变,原因是下列的________;
A.正逆反应都停止了
B.正反应速率为零
C.正逆反应速率相等,反应达到平衡状态
D.逆反应速率为零
(4)下列措施一定能使正反应速率增大的是______。
A.升高温度 B.降低温度
C.增大Y的浓度 D.减少Z的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为从海带中提取碘的工业生产过程,有关说法错误的是()
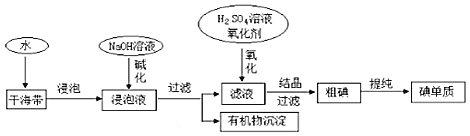
A.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等
B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀
C.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘
D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应的是
A. 2NaHCO3![]() Na2CO3+CO2↑+H2O B. Na2O+H2O=2NaOH
Na2CO3+CO2↑+H2O B. Na2O+H2O=2NaOH
C. 2KI+Br2=2KBr+I2 D. MgO+2HCl=MgCl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
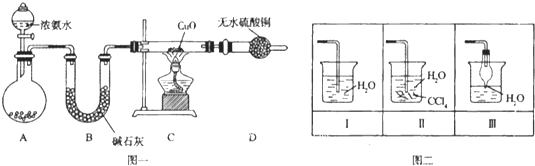
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属钠和镁,请根据下列工艺生产流程回答问题。

(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___。
(2)母液中加入石灰乳反应的离子方程式为__。
(3)若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,而MgO的熔沸点非常高,达到熔融状态需要消耗很多能源。所以,用电解法制取金属镁时,需要无水氯化镁。写出用电解法制取金属镁的化学方程式___。
(4)在以上提取镁的过程中,没有涉及的化学反应类型是__。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)小苏打可用于中和过多的胃酸,该反应的离子方程式为:___。
(2)向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀,变成海绵状的炭。蔗糖变黑,说明浓硫酸具有__性,后产生有刺激性气味的气体,说明浓硫酸具有___性。
(3)NO2是___色的有毒气体,它与水反应的化学方程式为___,该反应中氧化剂与还原剂的质量比为___。
(4)用10mol·L-1H2SO4配制480mL1mol·L-1H2SO4,有如下几个操作:
①计算并用量筒量取___mL10mol·L-1H2SO4稀释。
②配制溶液所用到的玻璃仪器除烧杯、玻璃棒外,还必须有__、__![]() 填仪器名称
填仪器名称![]() 。
。
③下列操作可能使所配溶液浓度偏小的是__![]() 填写序号
填写序号![]() 。
。
A.未洗涤烧杯和玻璃棒
B.定容时俯视容量瓶的刻度线
C.配溶液前容量瓶中有少量蒸馏水
D.摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)![]() CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是( )
CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是( )
A. ΔH2>ΔH3 B. ΔH1>ΔH3
C. ΔH2+ΔH3=ΔH1 D. ΔH1+ΔH2=ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.1molCH4 的质量为__________,分子数为__________(用NA表示,下同),原子总数为_________。
(2)500 mL 0.2 mol·L-1的Ba(NO3)2溶液中,NO3-的物质的量的浓度为______________,离子总数为_____________。
(3)在22 .2g某二价金属的氯化物中含有0 .4mol Cl-,此氯化物的摩尔质量为________,该金属元素的相对原子质量为__________。
(4)在标准状况下,由O2和O3组成的混合气体11.2 L,质量为20g。此混合物的平均摩尔质量是________,混合物中O2和O3的体积之比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com