
【题目】化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一.
(1)化学反应中有能量变化的本质原因是反应过程中有的断裂和形成.
(2)已知拆开1molH﹣H键、1molCl﹣Cl键、1molH﹣Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应 H2(g)+Cl2(g)=2HCl (g)的△H= .
(3)已知:CO(g)+ ![]() O2(g)═CO2(g)△H=﹣283.0kJ/mol CH3OH(l)+
O2(g)═CO2(g)△H=﹣283.0kJ/mol CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
(4)已知25℃、101kPa下,稀的强酸与稀的强碱溶液反应的中和热为﹣57.3kJ/mol. ①表示稀硫酸与稀烧碱溶液中和反应的热化学方程式为;
②测定中和热实验中所需的玻璃仪器有烧杯、量筒、环形玻璃搅拌棒、 .
【答案】
(1)化学键
(2)﹣185kJ/mol
(3)CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=﹣443.5kJ?mol﹣1
(4)![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;温度计
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;温度计
【解析】解:(1)化学反应的本质是化学键的断裂与形成,化学反应中能量变化的微观表现是断开化学键吸收的能量与形成化学键放出的能量不相等,若为若为放热反应,断开化学键吸收的能量小于形成化学键放出的能量,若为吸热反应,断开化学键吸收的能量大于形成化学键放出的能量,所以答案是:化学键;(2)已知拆开1molH﹣H键、1molCl﹣Cl键、1molH﹣Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应:H2(g)+Cl2(g)=2HCl(g)的△H=436kJ+243kJ﹣2×432kJ=﹣185KJ/mol;
所以答案是:﹣185kJ/mol;(3)①CO(g)+ ![]() O2(g)=CO2(g)△H=﹣283.0kJmol﹣1
O2(g)=CO2(g)△H=﹣283.0kJmol﹣1
②CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣726.5kJmol﹣1
O2(g)=CO2(g)+2H2O(l)△H=﹣726.5kJmol﹣1
依据盖斯定律②﹣①得到甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=﹣443.5kJmol﹣1 ;
所以答案是:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=﹣443.5kJmol﹣1 ;(4)①依据中和热概念分析,稀硫酸与稀烧碱溶液中和反应的热化学方程式为: ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3 kJ/mol;
Na2SO4(aq)+H2O(l)△H=﹣57.3 kJ/mol;
所以答案是: ![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3 kJ/mol;
Na2SO4(aq)+H2O(l)△H=﹣57.3 kJ/mol;
②依据量热计的结果和原理分析,测定中和热实验时所需的玻璃仪器有烧杯、量筒、温度计、环形玻璃搅拌棒;
所以答案是:温度计.
【考点精析】通过灵活运用反应热和焓变,掌握在化学反应中放出或吸收的热量,通常叫反应热即可以解答此题.


科目:高中化学 来源: 题型:
【题目】下列分子中,中心原子的杂化轨道类型相同,空间构型也相同的是( )
A.BeCl2 CO2
B.H2O SO2
C.BF3 NCl3
D.SiCl4 SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按照金属单质、混合物、氧化物的顺序排列的是 ( )
A. 水银、石灰石、过氧化氢 B. 氮气、空气、二氧化碳
C. 镁、海水、氧化钠 D. 铁、氢氧化钙、氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]化合物M是合成香精的重要原料。实验室由A和芳香烃E制备M的一种合成路线如下:

已知:![]()
请回答下列问题:
(1)A的化学名称为___________,F的结构简式为______________。
(2)B中官能团的名称为______________。
(3)F→G的反应类型为__________________。
(4)D+G→M的化学方程式为_________________。
(5)写出同时满足下列条件的D的同分异构体的结构简式___________。
①能发生水解反应和银镜反应
②不含环状结构
③核磁共振氢谱有4组峰
(6)参照上述合成路线和信息。以![]() 为原料(其他无机试剂任选),设计制备
为原料(其他无机试剂任选),设计制备 的合成路线______________________。
的合成路线______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研发出了一种新材料,其工作原理如图所示。在外接电源作用下,材料内部发生氧化还原反应导致颜色变化,从而实现对光的透过率进行可逆性调节。已知WO3和Li4Fe4[Fe(CN6]3均为无色透明,LiWO3和Fe4[Fe(CN6]3均有颜色。下列说法正确的是( )
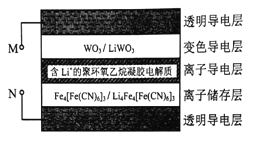
A. 当M外接电源正极时,该材料颜色变深使光的透过率降低
B. 该材料在使用较长时间后,离子导电层中Li+的量变小
C. 当M外接电源负极时,离子导电层中的Li+向变色导电层定向迁移
D. 当N外接电源正极时,离子储存层的电极反应式为:Fe4[Fe(CN6]3+4Li++4eˉ= Li4Fe4[Fe(CN6]3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 1.4gC2H4、C3H6的混合气体中,所含碳原子总数为0.lNA
B. 在0.1 mol·L Na2S溶液中,S2-、HS-、H2S微粒总数为0.1NA![]()
C. 标准状况下,22.4LC2H6中所含极性共价键的数目为7NA
D. 50mL l2mol·L的浓盐酸与足量MnO2反应,转移电子总数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是短周期周期表的一部分①~⑨是元素周期表的部分元素。

请回答下列问题:
(1) ③、⑤、⑥对应的原子半径最大的是_____(写元素名称)
(2)元素⑤和⑧形成的化合物的电子式是_____,该化合物溶于水被破杯的化学键类型为_______。
(3)元素⑥和⑨的最高价氧化物对应的水化物发生反应的离子方程式是________。
(4)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一稗常见的氧化剂,已知液态A与液态B充分反应生成已知液态10电子分子和一种气态单质,写出A与B反应的化学方程式:______________。
(5)某同学为了比较元素⑧和⑨非金属性的相对强弱,用如图所示装置进行实验:

①溶液c的作用是____________。
②溶液b是(填化学式)_____。写出溶液b中发生反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇属于可再生能源,可代替汽油作为汽车燃料,下列热化学方程式中的反应热能够正确表示甲醇燃烧热的是( )
A.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=+726.5kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+726.5kJ/mol
B.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
C.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(g)△H=﹣675.3kJ/mol
O2(g)═CO2(g)+2H2O(g)△H=﹣675.3kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1453kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com