
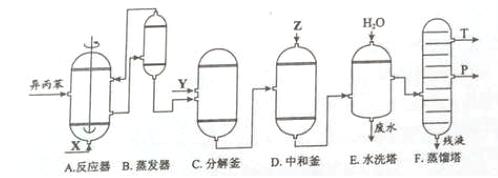
苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚
和丙酮,其反应和工艺流程示意图如下:
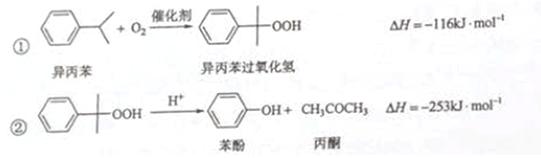
 [来源:学科网]
[来源:学科网]
相关化合物的物理常数
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 异丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
回答下列问题:
(1)在反应器A中通入的X是 。
(2)反应①和②分别在装置 和 中进行(填装置符号)。
(3)在分解釜C中加 入的Y为少置浓硫酸,其作用是______,优点是用量少,缺点是_______________。
入的Y为少置浓硫酸,其作用是______,优点是用量少,缺点是_______________。
(4)反应②为 (填“放热”或“吸热”)反应。反应温度控制在50-60℃,温度过高的安  全隐患是 。
全隐患是 。
(5)中和釜D中加入的Z最适宜的是 (填编号。已知苯酚是一种弱酸)
a. NaOH b. CaCO c. NaHCO d. CaO
(6)蒸馏塔F中的馏出物T和P分别为 和 ,判断的依据是 。
(7)用该方法合成苯酚和丙酮的优点是 。
科目:高中化学 来源: 题型:
向某一容积为5 L的密闭容器中,加入 0.2 mol CO和0.2 mol H2O,在800℃和催化剂的条件下,发生如下反应:CO(g)+H2O(g) 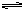 CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
(1)由图可知,反应从开始至达到平衡时,CO的化学反应速率v(CO)= ;H2的物质的量浓度c(H2)= ;该温度下此反应的平衡常数K= 。
(2)能说明该反应已达到平衡状态的是 (填序号)。
①CO、H2O、CO2、H2的浓度都相等
②密闭容器内压强保持不变
③CO减少的化学反应速率和CO2减少的化学反应速率相等
④CO、H2O、CO2、H2的浓度都不再发生变化
⑤密闭容器内密度保持不变
(3)若开始时向该容器中加入CO、H2O(g)、CO2和H2各0.1 mol,在相同条件下,反应达到平衡时,水蒸气的物质的量浓度c(H2O)= 。
(4)查表已知BaSO4(s)+4C(s)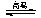 4CO(g)+BaS(s) △H1= +571.2 kJ·mol-1 ①
4CO(g)+BaS(s) △H1= +571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)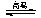 2CO2(g)+BaS(s) △H2= +226.2 kJ·mol-1 ②
2CO2(g)+BaS(s) △H2= +226.2 kJ·mol-1 ②
则反应C(s)+CO2(g)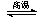 2CO(g)的△H= 。
2CO(g)的△H= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
[选修3—物质结构与性质]
19—Ⅰ(6分)下列物质的结构或性质与氢键无关的是
A.乙醚的沸点 B.乙醇在水中的溶解度
C.氢化镁的晶格能 D.DNA的双螺旋结构
19—Ⅱ(14分)钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2)钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴.阳离子个数分别为 . 。
(3)V2O5常用作SO2 转化为SO3的催化剂。SO2 分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个键。
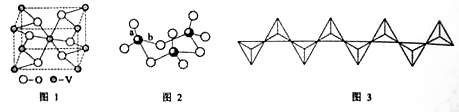
(4)V2O5 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
海水开发利用的部分过程如图所示。下列说法错误的是
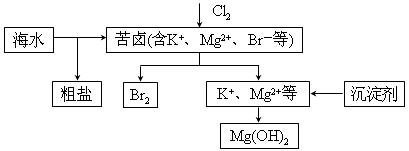
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有①0.112 L水 ②0.5NA个HCl分子
③25.6 g SO2气体 ④0.2 mol氨气 ⑤2 mol氦气 ⑥6.02×1023个白磷分子,所含原子个数从大到小的顺序为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由阿伏加德罗常数(NA)和一个水分子的质量(m水)、一个水分子的体积(V水)不能确定的物理量是________。
①1摩尔水的质量 ②1摩尔水蒸气的质量 ③1摩尔水蒸气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
由14CO和12CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),则下列关系正确的是( )
A.混合气体中,12CO占有的体积大于14CO占有的体积
B.混合气体中,12CO与14CO分子个数之比为1∶2
C.混合气体中,12CO与14CO质量之比为15∶14
D.混合气体中,12CO与14CO密度之比为14∶15
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com