
| A. | 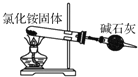 用装置来制备氨气 | |
| B. |  用装置来验证Cu与浓硝酸反应的热量变化 | |
| C. |  用装置来验证氨气极易溶于水 | |
| D. |  用装置来除去Cl2中混有的HCl气体 |
分析 A.氯化铵分解生成氨气和HCl,在试管口又化合生成氯化铵;
B.Cu与浓硝酸反应放热,大试管中空气受热膨胀;
C.氨气极易溶于水,烧瓶中气体减少;
D.氯气与水反应.
解答 解:A.氯化铵分解生成氨气和HCl,在试管口又化合生成氯化铵,图中装置不能制备氨气,应选铵盐与碱加热制备,故A错误;
B.Cu与浓硝酸反应放热,大试管中空气受热膨胀,则U型管中红墨水左低右高,装置可验证热量变化,故B正确;
C.挤压胶头滴管,氨气极易溶于水,烧瓶中气体减少,则气球变大,装置可验证氨气极易溶于水,故C正确;
D.氯气与水反应,不能除杂,应将水改为食盐水,食盐水可抑制氯气的溶解,故D错误;
故选AD.
点评 本题考查化学实验方案的评价,为高考常见题型,涉及反应中能量变化、混合物分离、物质的制备等基本实验,侧重于学生的分析能力、评价能力和实验能力的考查,注意把握实验的严密性和相关物质的性质,题目难度不大.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| B. | 1mol (NH4)2Fe(SO4)2•6H2O晶体中含有离子总数为5NA | |
| C. | 常温常压下,2.24 L SO2和O2的混合气体中含有的氧原子总数为0.2 NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中含的CO32-和HCO3-总数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2直线形 | B. | CO2平面三角形 | C. | BCl3三角锥形 | D. | CH4正四面体形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15 mol/L | B. | 0.225 mol/L | C. | 0.35 mol/L | D. | 0.45 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、油脂、蛋白质都能发生水解反应 | |
| B. | 蔗糖溶液中加入新制Cu(OH)2煮沸会析出砖红色沉淀 | |
| C. | 纤维素、淀粉都可用(C6H10O5)n表示,它们互为同分异构体 | |
| D. | 人体各种组织的蛋白质不断分解,最终生成二氧化碳和水,排出体外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解含CuSO4和NaCl的溶液,在阴极可能析出气体,阳极一定析出气体 | |
| B. | 电解CuCl2溶液可得到铜和氯气,阴极区酸性减弱,阳极区pH不变 | |
| C. | 碱性锌锰干电池的负极反应为:Zn-2e-+4OH-═ZnO22-+2H2O | |
| D. | 原电池负极金属一定比正极金属的金属性活泼 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com