
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)使用托盘天平称量药品,都不能直接放在托盘中,应放两张相同的纸片 ( )
(2)定容时,往容量瓶中缓慢加蒸馏水,等液面离容量瓶刻度线1~2 mL时,改用胶头滴管滴加蒸馏水 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
镍氢电池的总反应式是 H2+2NiO(OH)  2Ni(OH) 2 根据此反应式判断,此电池放电时,负极上发生反应的物质是 ( )
2Ni(OH) 2 根据此反应式判断,此电池放电时,负极上发生反应的物质是 ( )
A、NiO(OH) B、Ni(OH) 2 C、H2 D、H2和NiO(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是( )
A.Z与Y形成的化合物可作为耐高温材料
B.WY2能与碱反应,但不能与任何酸反应
C.原子半径按X、Y、Z、R、W的顺序依次增大
D.熔沸点:X2R>X2Y
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
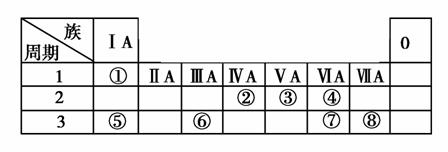
(1)请画出元素⑥的离子结构示意图:________________。
(2)元素⑦中质子数和中子数相等的同位素符号是______。
(3)④、⑤、⑦的简单离子半径由大到小的顺序为_______。
(4)②的最高价氧化物对应水化物的电离方程式为_______。
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为________________。
(6)由表中两种元素形成的5核10电子分子常做燃料电池的燃料,该电池在碱性条件下的负极反应式为________________。
(7)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知16 g液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,并放出838 kJ热量,写出A与B反应的热化学方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下下列说法正确的是:( )
A.Na,Mg,Al还原性依次减弱 B.HCl,PH3,H2S稳定性依次减弱
C.NaOH,KOH,CsOH碱性依次减弱 D.S2-,Cl-,Ca2+半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
关于元素周期表,下列叙述中不正确的是 ( )
A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B.在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素
C.在非金属元素区域可以寻找制备新型农药材料的元素
D.在地球上元素的分布和它们在元素周期表中的位置有密切关系
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨时一般采用700 K左右的温度,其原因是
①提高合成氨的速率 ②提高氢气的转化率③提高氨的产率 ④催化剂在700 K时活性最大
A.只有① B.①② C.②③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中, 作负极,发生 反应(选填“氧化”或“还原”),此电极反应式为 ;SO42-移向 极(选填“正”或“负”),利用该装置主要是将 能转化为 能。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com