
【题目】X、Y、Z、T、W五种元素的性质或原子结构如下表:
元素 | 元素性质或原子结构 |
X | 原子的最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 基态原子最外层电子排布式为(n+1)sn(n+1)pn+2 |
T | 与Z同周期,元素最高价是+7价 |
W | 原子序数为Y、T元素之和,不锈钢中含有该元素 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是;W元素基态原子电子排布式为 .
(2)元素Z与元素T相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 . A.常温下Z的单质和T的单质状态不同
B.T的氢化物比Z的氢化物稳定
C.一定条件下Z和T的单质都能与氢氧化钠溶液反应
D.T的电负性比Z大
(3)常见溶剂XZ2的分子中,含有的σ键与π键个数比为 , 它所形成的晶体类型为; Y的常见氢化物易液化的主要原因是
(4)①自然界常见的X元素含氧酸的钙盐和适量T的氢化物溶液反应时,每产生4.4g 气体(不考虑气体溶解)放热a kJ,则该反应的热化学方程式为 . ②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示
请用离子方程式表示BC段、CD段发生的反应:
BC段:;
CD段: .
【答案】
(1)C;1s22s22p63s23p63d54s1
(2)Cl;BD
(3)1:1;分子晶体;NH3分子间存在氢键
(4)CaCO3(s)+2HCl(aq)=CaCl2(aq)+CO2(g)+H2O(l)△H=﹣10aKJ/mol;Ca2++CO32﹣=CaCO3↓;CO32﹣+H2O?HCO3﹣+OH﹣、HCO3﹣+H2O?H2CO3+OH﹣
【解析】解:(1)元素X的一种同位素可测定文物年代,这种同位素的符号是C,Cr元素为24号元素,其原子核外有24个电子,其基态原子电子排布式为:1s22s22p63s23p63d54s1 , 所以答案是:C;1s22s22p63s23p63d54s1;(2)元素S与元素Cl为同周期的元素,同周期越向后非金属性越强,所以非金属性较强的是Cl;氢化物越稳定则非金属性越强,电负性越强则非金属性越强,所以答案是:Cl;BD;(3)常见溶剂CS2分子的结构式为S=C=S,则含有的σ键与π键个数比为1:1;CS2为分子晶体;N的氢化物为NH3分子间存在氢键,所以答案是:1:1;分子晶体;NH3分子间存在氢键;(4)①碳酸钙与HCl反应生成4.4g 二氧化碳气体(不考虑气体溶解)放热a kJ,则n(CO2)=0.1mol,所以生成1mol二氧化碳时放热为10aKJ,该反应的热化学方程式为CaCO3(s)+2HCl(aq)=CaCl2(aq)+CO2(g)+H2O(l)△H=﹣10aKJ/mol,所以答案是:CaCO3(s)+2HCl(aq)=CaCl2(aq)+CO2(g)+H2O(l)△H=﹣10aKJ/mol;②由图象可知BC段PH不变,则为CaCl2+Na2CO3=CaCO3↓+2NaCl,其离子方程式为:Ca2++CO32﹣=CaCO3↓;CD段碱性增强则为碳酸钠过量时,碳酸钠水解引起的,其水解方程式为:CO32﹣+H2OHCO3﹣+OH﹣、HCO3﹣+H2OH2CO3+OH﹣ , 所以答案是:;CO32﹣+H2OHCO3﹣+OH﹣、HCO3﹣+H2OH2CO3+OH﹣ .
【考点精析】利用非金属在元素周期表中的位置及其性质递变的规律对题目进行判断即可得到答案,需要熟知在目前已知的112种元素中,非金属元素有22种,除H外非金属元素都位于周期表的右上方(H在左上方).F是非金属性最强的元素.


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌.以下是过氧化氢法生产亚氯酸钠的工艺流程图: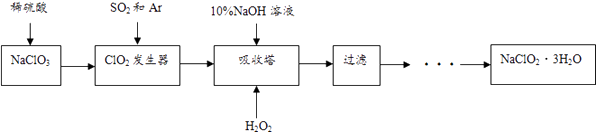
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO23H2O
②纯ClO2常温下为气体,易分解爆炸,一般用稀有气体或空气稀释到10%以下安全
(1)10%的NaOH溶液的密度为1.2g/cm3其物质的量浓度为 .
(2)在ClO2发生器中当1gSO2完全转化时,放出akJ热量,写出该热化学反应方程式鼓入Ar的作用是 .
(3)写出吸收塔内发生的化学反应方程式 . 吸收塔的温度不能超过40℃,其目的是 .
(4)从滤液中得到的NaClO23H2O粗晶体中往往含有杂质,要得到更纯的NaClO23H2O晶体方法是 .
(5)工业处理含NaClO2废水时,先向废水中加入适量NaOH,用惰性电极电解该废水,同时制得NaClO3 , 写出ClO2﹣在阳极放电时的电极反应方程式 .
(6)已知SO2和Ar的混合气体中,SO2的百分含量为5.6a%,当bL(标况下)该混合气体参加反应时,理论上需要的17%的H2O2的质量为g(结果必须化简).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表的叙述中正确的是( )
A. 元素周期表有7个周期和18个族
B. 由短周期元素和长周期元素共同组成的族一定是主族
C. 从左向右数第13列是第ⅢB族
D. 元素周期表中0族元素的单质全部是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,某同学对该固体进行了如下实验,下列判断正确的是( ) 
A.白色沉淀乙不一定是Al(OH)3
B.气体甲一定是纯净物
C.固体X中一定存在(NH4)2SO4、MgCl2
D.固体X中一定存在FeCl2、AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的反应P(g)+Q(g)![]() R(g)+S(g)下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+S(g)下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
A. P、Q、R、S的浓度相等
B. P 、Q、R、S在密闭容器中共存
C. P、Q、R、S的浓度不再变化
D. 用P的浓度变化表示的化学速率与用Q的浓度表示的化学反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的资源化利用是解决温室效应的重要途径,如图是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应: 
下列有关三聚氰酸的说法正确的是( )
A.分子式为C3H6N3O3
B.分子中既含极性键,又含非极性键
C.属于共价化合物
D.生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)下图为四种粒子的结构示意图,完成以下填空: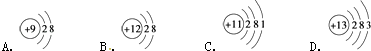
属于阳离子结构的粒子是(填字母序号,下同);A粒子的半径B粒子的半径(填“>”、“<”或“=”).
(2)有机物M经过太阳光光照可转化成N,转化过程如下: 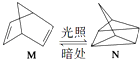 △H=+88.6kJmol﹣1则M、N相比,较稳定的是 .
△H=+88.6kJmol﹣1则M、N相比,较稳定的是 .
(3)由氢气和氧气反应生成1mol水蒸气放出热量241.8kJ,写出该反应的热化学方程式为: .
(4)一定温度下在某定容容器中发生反应:2A(g)+3B(g)2C(g),开始时,A的浓度为2molL﹣1 , B的浓度为4molL﹣1 , 2min后,A的浓度减少0.8molL﹣1 , 则①v(B)= , v(C)= .
②在2min末,C的浓度是 , B的浓度是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)中一种重要的掺杂剂.实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3 , 装置如下图所示:(部分夹持装置略去)
已知黄磷与少量Cl2反应生成PCl3 , 与过量Cl2反应生成PCl5和HCl,遇O2会生成POCl3 , POCl3溶于PCl3 , PCl3、POCl3的熔沸点见下表:
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | ﹣112 | 75.5 |
PCl5 | 2 | 105.3 |
请回答下列问题
(1)装置中制氯气的离子方程式为
(2)B中的试剂是 , E中次冷水的作用是 , F中碱石灰的作用是
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2 , 再迅速加入黄磷.通干燥CO2的作用是通过控制K1、K2能除去A、B装置中的空气,具体的方法是
(4)粗产品含有POCl3、PCl3等,加入黄磷加热除去PCl5 , 通过(填实验操作的名称),即可得到纯净的PCl3
(5)通过下面方法可测定产品中PCl3的质量分数.①迅速称取100g产品,加水反应后配成250mL溶液;
②取以上溶液25.0mL,向其中加入0.1mol 10mL碘水,充分反应;③向②所得溶液中加入几滴淀粉溶液,用0.1mol/L的Na2S2O3溶液滴定,滴定终点现象是
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.已知H3PO3+H2O+I2=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2SO4根据以上数据,该产品中PC3的质量分数是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com