
【题目】50mL浓硫酸和铜片加热后反应,铜片完全溶解后测得产生4.48L(标况下)气体,把反应后的溶液稀释至1L,取20mL溶液加入足量BaCl2溶液产生3.262g沉淀,求原硫酸溶液的物质的量浓度是多少______?
【答案】18mol/L
【解析】
硫酸中S元素一部分变为SO2,一部分仍以SO42-形成存在溶液中,先计算SO2、剩余SO42-的物质的量,然后根据c=![]() 计算原硫酸的物质的量浓度。
计算原硫酸的物质的量浓度。
Cu与浓硫酸发生反应:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,反应产生的SO2的物质的量为n(SO2)=
CuSO4+SO2↑+2H2O,反应产生的SO2的物质的量为n(SO2)=![]() =
=![]() =0.2mol,反应后溶液中硫酸铜及未反应的硫酸电离产生的SO42-与加入的BaCl2溶液发生离子反应:Ba2++ SO42-=BaSO4↓,在1L反应后溶液中含有的SO42-的物质的量为n(SO42-)=
=0.2mol,反应后溶液中硫酸铜及未反应的硫酸电离产生的SO42-与加入的BaCl2溶液发生离子反应:Ba2++ SO42-=BaSO4↓,在1L反应后溶液中含有的SO42-的物质的量为n(SO42-)=![]() =0.7mol,则根据S元素守恒,可知原浓硫酸中含有硫酸的物质的量为n(H2SO4)=n(SO42-)+n(SO2)=0.7mol+0.2mol=0.9mol,所以c(H2SO4)=
=0.7mol,则根据S元素守恒,可知原浓硫酸中含有硫酸的物质的量为n(H2SO4)=n(SO42-)+n(SO2)=0.7mol+0.2mol=0.9mol,所以c(H2SO4)=![]() =18mol/L。
=18mol/L。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.分子内共价键越强,分子越稳定,其形成的晶体的熔沸点也越高
B.离子键的本质就是阴、阳离子之间的相互吸引
C.金刚石转化为石墨的过程中不存在化学键被破坏的过程
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应3A(g)+2B(g) ![]() 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,化学平衡常数增大
D. 增加B,B的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
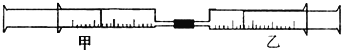
实验序号 | 甲针筒内物质 | 乙针筒内物质 |
1 | 溴水 | SO2 |
2 | H2S | SO2 |
3 | NO2(主要) | H2O(l) |
4 | 15mLCl2 | 40mLNH3 |
试回答下列问题:
(1)实验1中,溶液颜色由______色变为______色,写出溶液变色的化学反应方程式____________。
(2)实验2甲针筒内发生的化学反应方程式:_______________。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入________溶液中。
(3)实验3中,甲中最后剩余的无色气体是_____,写出NO2与H2O反应的化学反应方程式_____________。
(4)实验4中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式______________,写出检验所得白色固体中阳离子的操作方法:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明硫元素的非金属性弱于氯元素的事实是( )
A. 通常情况下硫为浅黄色固体,而氯气为黄绿色的气体
B. 硫不溶于水而氯气溶于水
C. 跟金属或氢气反应时,硫被还原为![]() 价,而氯被还原为
价,而氯被还原为![]() 价
价
D. 跟Cu或Fe反应时,金属被硫氧化成低价态,而被氯气氧化成高价态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池
B.锌锰干电池中,锰是正极,锌是负极
C.甲醇燃料电池可把化学能转化为电能
D.铅蓄电池中,正极板上覆盖的是PbO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com