
氧化还原反应在生产、生话中应用广泛,用所学知识回答问题:
(1)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2,该反应的化学方程式为 ,反应中消耗1mol的H2C2O4时转移电子数为
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol
(3)写出Na2S与FeCl3溶液混合的离子方程式 .
| 氧化还原反应;离子方程式的书写. | |
| 分析: | (1)酸性条件下KMnO4与H2C2O4发生氧化还原反应生成MnSO4和CO2,根据方程中反应中KMnO4与H2C2O4的计量数关系,结合Mn元素化合价由+7价降低到+2价计算; (2)n(KI)=0.06mol,与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则n(I2)=n(KIO3)=0.02mol,结合化合价的变化计算转移的电子的数目,可计算消耗KMnO4的物质的量; (3)FeCl3和Na2S溶液混合发生氧化还原反应,铁离子氧化硫离子为单质硫. |
| 解答: | 解:(1)酸性条件下KMnO4与H2C2O4发生氧化还原反应生成MnSO4和CO2,反应的化学方程式为2KMnO4+5H2C2O4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O,反应中消耗1mol的H2C2O4时,KMnO4为0.4mol,反应中Mn元素化合价由+7价降低到+2价,反应中消耗0.4mol的MnO4﹣时转移电子0.4mol×5=2mol,则电子数为2NA, 故答案为:2KMnO4+5H2C2O4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O;2NA; (2)n(KI)=0.06mol,与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则n(I2)=n(KIO3)=0.02mol,共失去电子的物质的量为2×0.02mol+0.02mol×[5﹣(﹣1)]=0.16mol,则消耗KMnO4的物质的量的是 故答案为:0.032; (3)FeCl3和Na2S溶液混合发生氧化还原反应,铁离子氧化硫离子为单质硫,离子方程式为2Fe3++S2﹣=2Fe2++S↓; 故答案为:2Fe3++S2﹣=2Fe2++S↓. |
| 点评: | 本题考查较为综合,涉及氧化还原反应以及物质的含量的测定,侧重于学生的分析能力和计算能力的考查,为高考常见题型,注意根据反应的相关化学方程式或离子方程式解答该题,难度中等. |


科目:高中化学 来源: 题型:
已知吡啶()与苯环性质相似。有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成
部分。下列说法不正确的是 ( )
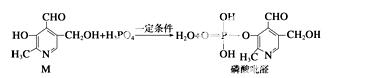
A.M能使酸性高锰酸钾溶液褪色
B.1 mol磷酸吡醛与足量的金属钠反应,最多消耗3 mol Na
C.1 mol磷酸吡醛与NaOH溶液反应,最多消耗3 mol NaOH
D.M与足量H2反应后所得有机物的分子式为C8H17O3N
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应与四种基本类型反应的关系如右图所示,则下列化学反应属于3 区域的是
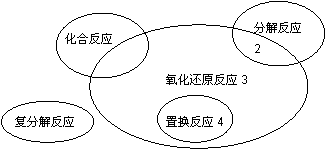 |
|
|
B.2NaHCO3 Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O 4Fe(OH)3
D.2Na2O2+2CO2 2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的Fe、FeO、Fe3O4和Fe2O3的混合物中加入250mL 4mol/L的稀硝酸,恰好使混合物完全溶解.放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现,若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
|
| A. | 0.21mol | B. | 0.25mol | C. | 0.45mol | D. | 0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是( )
|
| A. | 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I﹣、Br﹣、Fe2+ |
|
| B. | 在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+、Fe2+ |
|
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3 |
|
| D. | 在含等物质的量的AlO2﹣、OH﹣、CO32﹣溶液中,逐滴加入盐酸:AlO2﹣、Al(OH)3、OH﹣、CO32﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
用二氧化氯、铁酸钠(Na2FeO4)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术,ClO2和Na2FeO4在水处理过程中分别被还原为Cl﹣和Fe3+.
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 > >
(2)Na2FeO4溶于水会放出一种无色无味气体,其杀菌消毒、吸附水中的悬浮杂质的原理可用离子方程式表示为
(3)工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3﹣+2Cl﹣+4H+=2ClO2↑+Cl2↑+2H2O
①写出第二步反应的离子方程式
②工业生产时需在反应物中加少量Cl﹣,其作用是
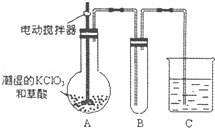
(4)已知二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为﹣59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸在60℃时反应制得,ClO2也可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.某学生用如图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置.请问:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置
②C中应装的试剂为 C中发生反应的化学方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是制取乙酸乙酯的装置,下列说法中错误的是( )。
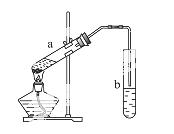
A.浓硫酸在此反应中作为催化剂、吸水剂
B.b中导气管不能插入饱和碳酸钠溶液中,目的是防止倒吸
C.试管a中加入碎瓷片目的是防止剧烈沸腾
D.先向试管a中加入浓硫酸,然后依次加入酒精、乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对某黄铁矿石进
行如下实验探究。
[实验一]测定硫元素的含量。
Ⅰ、将m1 g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2
|
 2Fe2O3+8SO2
2Fe2O3+8SO2 
Ⅱ、反应结束后,将乙瓶中的溶液进行如下处理:

|
III、测定铁元素含量的实验步骤如图所示。


问题讨论:
(1)I中,甲瓶内所盛试剂是____溶液。乙瓶内发生反应的离子方程式为____。
(2)II中,乙瓶加入H2O2溶液时反应的离子方程式为_____________________。
(3)该黄铁矿中硫元素的质量分数为_______________________。
(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有____________________________________________。
(5)III的步骤④中,表示滴定已达终点的现象是
(6)Ⅲ的步骤④进行了三次平行实验,测得消耗KMnO4溶液体积分别为24.98mL、24.80mL、25.02mL(KMnO4被还原为Mn2+)。根据上述数据,可计算出该黄铁矿样品铁元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与实验相关的叙述正确的是
A.用苯萃取溴水中的Br2时,有机层从分液漏斗的下端放出
B.检验溶液中是否含有SO42-:依次滴入Ba(NO3)2溶液和稀盐酸
C.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
D.配制AlCl3溶液时,将AlCl3溶解在较浓的盐酸中,再用水稀释到所需浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com