
| A. | 升高温度,促进c(CO32-)水解,pH增大 | |
| B. | 离子浓度:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| C. | 离子浓度:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 离子浓度:c(Na+)>c(CO32-)>c(H+)>c(OH-)>c(HCO3-) |
分析 A.碳酸钠溶液中碳酸根离子水解溶液显碱性,水解过程是吸热反应;
B.溶液中存在物料守恒,n(Na)=2n(C),碳元素物质的量所有存在形式总和等于钠元素物质的量;
C.溶液中存在电荷守恒分析判断选项;
D.碳酸根离子分步水解,溶液显碱性,据此分析离子浓度大小;
解答 解:A.碳酸钠溶液中碳酸根离子水解溶液显碱性,水解过程是吸热反应,加热促进水解正向进行,溶液碱性增强,溶液PH增大,故A正确;
B.溶液中存在物料守恒,n(Na)=n(C),离子浓度:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故B正确;
C.溶液中存在电荷守恒c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故C错误;
D.碳酸根离子分步水解,溶液显碱性,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,离子浓度大小为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故D错误;
故选AB.
点评 本题考查了盐类水解的原理,电解质溶液中电荷守恒、物料守恒、离子浓度大小比较,注意碳酸根离子分步水解,题目难度中等.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 含1mol FeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6 g Na与足量的稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 1L 0.1mol•L-1的Na2CO3中CO32-数目小于0.1 NA | |
| D. | 常温下,22g CO2含碳氧双键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
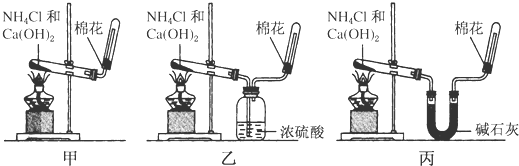
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
| B | 将铜粉加入1.0mol/L Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,可以通过观察气泡多少来比较不同浓度Na2SO3溶液与稀H2SO4溶液反应的快慢 | |
| B. | 实验室制取乙酸乙酯时,向试管中加入乙醇,然后边摇动试管边慢慢加入浓硫酸和冰醋酸 | |
| C. | 用已知浓度NaOH溶液滴定未知浓度盐酸,滴定终点时,俯视刻度线,则测得盐酸浓度偏小 | |
| D. | 用洗净铂丝蘸取未知溶液进行焰色反应,呈黄色火焰,则该溶液有Na+,无K+的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在豆浆里加入盐卤做豆腐,在河流入海处易形成沙洲都与胶体性质有关 | |
| B. | 淀粉胶体中混有的氯化钠可以通过渗析的方法除去 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 | |
| D. | Fe(OH)3悬浊液和Fe(OH)3胶体都不稳定,都不能透过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不用试剂就可以鉴別Al(OH)3胶体和食盐水 | |
| B. | 签别NO2和Br2蒸汽,可以用AgNO3溶液 | |
| C. | 鉴别粉笔木与水、豆油与水组成的浊液,可以不用任何试剂 | |
| D. | 鉴别NaCl与Na2S04两种溶液,可以用AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol SO2的质量为64g/mol | |
| B. | 10g H2和10g O2含有相同的分子数 | |
| C. | 23g钠在氧气中完全燃烧失去电子数为NA | |
| D. | 标准状况下,11.2LH2O所含分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com