

分析 (1)根据锌的质量计算生成气体的体积,从而确定量气管的适宜规格;
(2)氢氧化钠溶液质量增重,说明生成酸性气体,说明反应生成二氧化硫;
(3)1 mol锌无论用来产生SO2 还是产生氢气都是1 mol锌对应1 mol气体;
(4)氢氧化钠洗气瓶增重的量求出反应的硫酸的物质的量,硫酸总量减去生成二氧化硫需要的硫酸的量即为生成氢气的硫酸的量,继而求出生成气体的物质的量;无水氯化钙起到吸水的作用;
(5)读数时应避免实验误差,且避免温度的影响,在常温下,且液面、实现水平相切.
解答 解:(1)设生成的氢气体积为xL,
Zn+H2SO4=ZnSO4+H2↑
1mol 22.4L
$\frac{1.30g}{65g/mol}$=0.02mol x
则x=0.448L=448mL,则量气管的规格应该选500mL,
故答案为:C;
(2)氢氧化钠是碱,能吸收酸性气体,氢氧化钠洗气瓶增重说明有酸性气体生成,当锌和硫酸反应时,锌作还原剂,硫酸作氧化剂,被还原为二氧化硫,由(1)计算可知,1.30g锌和硫酸反应若只生成二氧化硫,共生成0.02mol,质量为0.02mol×64g/mol=1.28g,与氢氧化钠增重的质量一致,故发生反应的化学方程式为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O,
故答案为:Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O;
(3)根据氧化还原知识或根据方程式,1 mol锌无论用来产生SO2 还是产生氢气,都是1mol锌对应1 mol气体,根据氧化还原反应中得失电子数相等可得:$\frac{ag}{65g/mol}$=$\frac{bg}{64g/mol}$+$\frac{VL}{22.4mL/mol}$,
故答案为:$\frac{ag}{65g/mol}$=$\frac{bg}{64g/mol}$+$\frac{VL}{22.4mL/mol}$;
(4)Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O
2mol 1mol
$\frac{m}{32}$mol $\frac{m}{64}$mol
则生成二氧化硫需要的硫酸为$\frac{m}{32}$mol;
Zn+H2SO4=ZnSO4+H2↑
1mol 1mol
( cV-$\frac{m}{32}$)mol (cV-$\frac{m}{32}$)mol
则:$\frac{n(H{\;}_{2})}{n(SO{\;}_{2})}$=$\frac{(cV-\frac{m}{32})mol}{\frac{m}{64}mol}$=$\frac{64cV-2m}{m}$;
若撤走盛有无水氯化钙的U型管,混合气体中的水蒸气进入氢氧化钠溶液,导致洗气瓶增重量增大,所以计算时二氧化硫的物质的量增大,氢气与二氧化硫的物质的量之比偏小,
故答案为:$\frac{64cV-2m}{m}$;偏小;
(5)因为该反应是放热反应,随着反应的进行,溶液的温度逐渐升高,生成的气体温度高于标况下温度,温度对气体体积有影响,所以要待冷却至室温才开始读数;在读数时,如果俯视或仰视都会造成误差,所以读数时眼睛视线与液面最低处相平,
故答案为:①待冷却至室温才开始读数;②读数前使量气管左右液面相平;③视线与量气管中液面的凹液面最低点在同一水平面.
点评 本题考查了浓硫酸的性质,题目难度中等,明确发生反应原理为解答关键,注意掌握电子守恒在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学实验能力.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:解答题
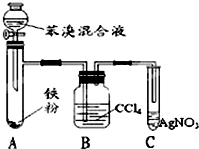 如表是A、B、C三种烃的有关信息;
如表是A、B、C三种烃的有关信息;| A | B | C |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  | 1棍模型为: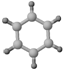 ②平面型结构 | ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与H2在一定条件下反应生成A |
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ④⑤⑥ | D. | ②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L Na2CO3溶液中的Na+数目为2NA | |
| B. | 标准状况下,1 molCH2Cl2所占有的体积约为22.4L | |
| C. | 常温常压下,38g 18OH-中含质子数20NA | |
| D. | 14g C2H4和C3H6的混合气体含有的原子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
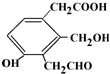 ,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.
,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.4g氨气中含有0.6NA个N-H键 | |
| B. | 78g Na2O2晶体中所含阴阳离子个数均为4NA | |
| C. | 只含有共价键的物质一定是共价化合物 | |
| D. | PCl3和H2O分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
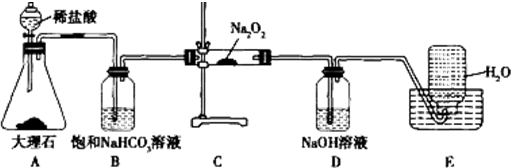
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
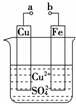
| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu | |
| C. | a和b用导线连接时,电子由铜电极流向铁电极 | |
| D. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com