
从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学变化的是 ( )
①对空气进行降温加压 ②金刚石变成石墨 ③NaCl熔化 ④碘溶于CCl4中 ⑤HCl溶于水电离出H+和Cl- ⑥电解熔融的Al2O3制取Al
A.②③⑤ B.②⑤⑥
C.②⑥ D.②③⑤⑥
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
下列反应属于取代反应的是 ( )。
①CH3CH===CH2+Br2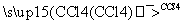 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH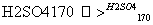 CH2===CH2↑+H2O
CH2===CH2↑+H2O
③CH3COOH+CH3CH2OH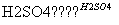 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3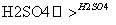 C6H5NO2+H2O
C6H5NO2+H2O
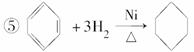
⑥2CH3CH2OH+O2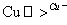 2CH3CHO+2H2O
2CH3CHO+2H2O
⑦纤维素最终水解生成葡萄糖
⑧油脂的皂化反应
⑨氨基酸生成多肽的反应
⑩nCH2===CH2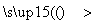 CH2—CH2
CH2—CH2
A.③④⑦⑧ B.①②③④
C.⑤⑥⑦⑧ D.③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生对SO2与漂粉精的反应进行实验探究:
| 操 作 | 现 象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
|
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是___________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是________。
(3)向水中持续通入SO2,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是________。
②由实验a、b不能判断白雾中含有HCl,理由是____________________________。
(4)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是________。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某气态烷烃20 mL,完全燃烧时,正好消耗同温同压下的氧气100 mL,该烃的化学式是( )。
A.C2H6 B.C3H8
C.C4H10 D.C5H12
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误(正确打“√”,错误的打“×”,并改正)
(1)Na2S [Na+] 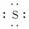
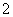 [Na+]( )
[Na+]( )
(2)Na2O Na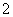 [
[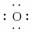 ]2-( )
]2-( )
(3)MgBr2 Mg2+[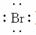 ]
]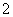 ( )
( )
(4)H2O H+[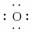 ]2-H+( )
]2-H+( )
(5)OH- 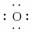 H( )
H( )
(6)HClO H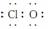 ( )
( )
(7)Cl2 ClCl( )
(8)O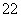 [
[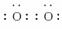 ]2-( )
]2-( )
(9)羟基 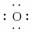 H( )
H( )
(10)H2S H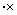
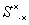
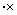 H( )
H( )
(11)Na+ [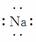 ]+( )
]+( )
(12)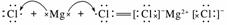 ( )
( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
A.SO3和SiO2 B.CO2和H2O
C.NaCl和HCl D.CCl4和KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
A.离子键 B.共价键
C.一种静电引力 D.一种静电斥力
查看答案和解析>>
科目:高中化学 来源: 题型:
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是 ( )。

A.电解时电子从电源负极→导线→铝极,铅极→导线→电源正级
B.在电解过程中,H+向阳极移动,SO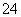 向阴极移动
向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:2CH3OH(g)CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。在此温度下,向密闭容器中加入一定量CH3OH,反应到5 min时测得各组分的浓度如表所示:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
(1)该反应在低温下(此时水为液态)能自发进行,则该反应的ΔH______0(填“>”、“<”或“=”,下同)。
(2)比较此时正、逆反应速率的大小:v正______v逆。
(3)前5 min时,用CH3OCH3表示该反应的速率为________________。
(4)再过一段时间后,反应达到平衡状态。能判断该反应已达到化学平衡状态的依据是__________(填字母)。
A.容器中压强不变
B.混合气体中c(CH3OH)不变
C.v生成(CH3OH)=2v消耗(H2O)
D.c(CH3OCH3)=c(H2O)
(5)达到平衡状态时,CH3OH的转化率为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com