
���� ��1���ٸ���ʱ������������̷����û���Ӧ�����̣�Ϊ���ȷ�Ӧ��
�ڸ����ṩ�ķ�Ӧ��Ͳ��P������ԭ��Ӧ��֪Mn��+4�۱�Ϊ+2�ۣ���Ԫ�ػ��ϼۿ϶����ߣ�
��2��Fe��������ȼ�������Ȼ�����ȡ����X��Һ���ݣ�һ�ݼ���KSCN��Һʱ����Һ�Ժ�ɫ����X�к�Fe3+����һ���м����ɫ���軯�� ��K3[Fe��CN��6]����Һ���ܷ������ֽⷴӦ������ɫ��������X�л������л�ԭ�Ե�Fe2+����Fe�������ķ�Ӧ��Fe�������Դ˽��
��3��15.6gNa2O2�����ʵ���Ϊ$\frac{15.6g}{78g/mol}$=0.2mol��5.4gAl�����ʵ���Ϊ$\frac{5.4g}{27g/mol}$=0.2mol��6.72LHCl��������ʵ���Ϊ$\frac{6.72L}{22.4L/mol}$=0.3mol���ȼ���������ơ�����HCl�����ʵ����������÷����Ļ�ѧ��Ӧ��2Na2O2+2H2O�T4NaOH+O2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����NaOH+HCl�TNaCl+H2O��NaAlO2+HCl+H2O�TAl��OH��3��+NaCl���������
��� �⣺��1���ٸ���ʱ������������̷����û���Ӧ�����̣���Ӧ�ķ���ʽΪ3MnO2+4Al$\frac{\underline{\;����\;}}{\;}$3Mn+2Al2O3��
�ʴ�Ϊ��3MnO2+4Al$\frac{\underline{\;����\;}}{\;}$3Mn+2Al2O3��
�ڸ���������ԭ��Ӧ��֪Mn��+4�۱�Ϊ+2�ۣ������ϼۿ϶����ߣ����Բ������������ɣ���ӦΪMnO2+H2O2+2H+�TMn2++O2��+2H2O��
�ʴ�Ϊ��MnO2+H2O2+2H+�TMn2++O2��+2H2O��
��2��Fe��������ȼ�������Ȼ�����ȡ����X��Һ���ݣ�һ�ݼ���KSCN��Һʱ����Һ�Ժ�ɫ����X�к�Fe3+����һ���м����ɫ���軯�� ��K3[Fe��CN��6]����Һ���ܷ������ֽⷴӦ������ɫ��������X�л������л�ԭ�Ե�Fe2+����Fe�������ķ�Ӧ��Fe������
��������������֪��X�к���������ΪFe3+��Fe2+�������ķ�Ӧ�У�2Fe+Cl2$\frac{\underline{\;��ȼ\;}}{\;}$2FeCl3��2FeCl3+Fe=3FeCl2��
�ʴ�Ϊ��2Fe+Cl2$\frac{\underline{\;��ȼ\;}}{\;}$2FeCl3��2FeCl3+Fe=3FeCl2��
����ɫ�����������軯����ͼ�̬�����ӷ�Ӧ�Ľ�����ͼ�������Ϊ�������ӣ���Ӧ�����ӷ���ʽΪ��3Fe2++2[Fe��CN��6]3-=Fe3[Fe��CN��6]2����
�ʴ�Ϊ��3Fe2++2[Fe��CN��6]3-=Fe3[Fe��CN��6]2����
��3��15.6gNa2O2�����ʵ���Ϊ$\frac{15.6g}{78g/mol}$=0.2mol��5.4gAl�����ʵ���Ϊ$\frac{5.4g}{27g/mol}$=0.2mol��6.72LHCl��������ʵ���Ϊ$\frac{6.72L}{22.4L/mol}$=0.3mol��
2Na2O2+2H2O�T4NaOH+O2��
0.2mol 0.4mol 2.24L
2Al+2H2O+2NaOH�T2NaAlO2+3H2��
0.2mol 0.2mol 0.2mol 6.72L
��Ȼ�������ƹ���������ȫ��Ӧ��
�ٷ�Ӧ�й��õ���������Ϊ��2.24L+6.72L=8.96L��
�ʴ�Ϊ��8.96L��
�ڽ�15.6gNa2O2��5.4gAlͬʱ����һ������ˮ�У���Ӧ����Һ�ijɷ�Ϊ0.2molNaOH��0.2molNaAlO2������0.3molHCl��0.2mol������������0.2mol�Ȼ��⣬ʣ���0.1mol�Ȼ�����ƫ�����Ʒ�ӦNaAlO2+HCl+H2O�TAl��OH��3��+NaCl����0.1mol��������������
���ɵ���������������Ϊ��78g/mol��0.1mol=7.8g��
�ʴ�Ϊ���ǣ�7.8g��
���� ���⿼���˽������仯�������ʵ��ۺ�Ӧ�á����ӷ���ʽ�ļ��㣬��Ŀ�Ѷ��еȣ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ѧ����������ע�����ճ����������ʼ��仯�������ʣ��ܹ����ݸ��ݷ����ķ�Ӧ�����ؼ��㣮


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д� ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ú��ʯ�ͺ���Ȼ��Ϊ��Ҫԭ�������ĺϳɲ��������ϡ��ϳ����ϳ���ά | |
| B�� | ú�ǹ�ҵ�ϻ�÷�������һ����Ҫ��Դ | |
| C�� | ʯ�͵��ѽ���Ϊ����������ͣ��������ͣ��IJ��� | |
| D�� | ��Ȼ������Ҫ�ɷ��Ǽ��飬���ڲ���������Դ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ӻ�����һ���������Ӽ� | |
| B�� | ���ۻ�����һ���������Ӽ� | |
| C�� | ֻ�����ۼ������ʽй��ۻ����� | |
| D�� | ��ѧ��Ӧ�Ĺ��̣��������Ǿɻ�ѧ�����Ѻ��»�ѧ���γɵĹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
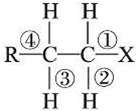
| A�� | ����ˮ�ⷴӦʱ�����ƻ��ļ��Ǣٺ͢� | |
| B�� | ������ȥ��Ӧʱ�����ƻ��ļ��Ǣٺ͢� | |
| C�� | ����ˮ�ⷴӦʱ�����ƻ��ļ��Ǣٺ͢� | |
| D�� | ������ȥ��Ӧʱ�����ƻ��ļ��Ǣٺ͢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | BF3 | C�� | CO2 | D�� | N2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ﵽ��ѧƽ��ʱ�����ʹ�ϵΪ��v��NH3����v��O2����v��NO����v��H2O��=4��5��4��6 | |
| B�� | ����λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ��ƽ��״̬ | |
| C�� | �ﵽ��ѧƽ��ʱ�������������������Ӧ���ʼ�С���淴Ӧ�������� | |
| D�� | �ﵽ��ѧƽ��ʱv����O2����v�棨NO��=5��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ���� | ѡ���Լ� | ��ѧ����ʽ |
| FeCl2��Һ | FeCl3 | ���� | Fe+2FeCl3=3FeCl2 |
| SiO2 | Al 2O3 | ���� | Al2O3+6HCl=2AlCl3+3H2O |
| Fe��OH��3 | Al��OH��3 | NaOH��Һ | Al��OH��3+NaOH=Na[Ai��OH��4] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HI | B�� | HBr | C�� | HCl | D�� | HF |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com