
【题目】用铂电极电解100mLHNO3 与AgNO3 的混合液,通电一段时间后,两极均收集到4.48L气体(标准状况),则原混合液中Ag+的物质的量浓度为( )
A. 1mol·L-1B. 2mol·L-1C. 2.5mol·L-1D. 4mol·L-1
【答案】D
【解析】
铂电极为惰性电极,电解HNO3与AgNO3的混合溶液,通电一段时间后,两极均收集到4.48L气体(标准状况),阴极发生2Ag++2e-=2Ag、2H++2e-=H2↑,阳极发生4OH--4e-=2H2O+O2↑,以此进行计算。
铂电极为惰性电极,电解HNO3与AgNO3的混合溶液,通电一段时间后,两极均收集到4.48L气体(标准状况),n(气体)=![]() =0.2mol,由阳极发生4OH--4e-=2H2O+O2↑可知,生成0.2molO2转移0.8mol电子,根据电子守恒可知,阴极转移0.8mol电子,则:
=0.2mol,由阳极发生4OH--4e-=2H2O+O2↑可知,生成0.2molO2转移0.8mol电子,根据电子守恒可知,阴极转移0.8mol电子,则:
2H++2e-=H2↑
0.4mol 0.2mol
2Ag++2e-=2Ag
0.4mol 0.4mol
即n(Ag+)=0.4mol,
则原混合溶液中Ag+的物质的量浓度为![]() =4mol/L,故答案为D。
=4mol/L,故答案为D。


科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
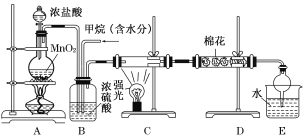
试回答下列问题:
(1)请写出C装置中生成CH3Cl的化学反应方程式:______________________________。
有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法________(填“正确”或 “不正确”)。
(2)B装置有三种功能;①控制气流速度;②混匀混合气体;③________。
(3)一段时间后发现D装置中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(4)E装置中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母)。
A.分液法 B.蒸馏法 C.结晶法
(5)将1molCH4与Cl2发生取代反应,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为 ,生成HCl的物质的量共为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用等体积的0.1mol/L的AgNO3溶液,可使相同物质的量浓度的NaCl、MgCl2和AlCl33种溶液中的Cl-恰好完全沉淀,则3种氯化物溶液的体积之比为( )
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的近似值为6.02×1023。按要求完成下列填空:
(1)1molCl2中约含有___个氯气分子,约含有__个氯原子。含有6.02×1023个氢原子的H2SO4的物质的量是___;
(2)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是___。
(3)2L1mol/LMgCl2中镁离子的物质的量为___,Cl-的物质的量浓度为___。
(4)三种盐的混合溶液中含有0.2molNa+、0.25molMg2+、0.4molCl-、SO42-,则SO42-的微粒个数约为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是
![]()
A. Y的原子半径比X的大
B. Q的最高价氧化物的水化物的酸性比Z的强
C. X、Y和氢3种元素形成的化合物中都只有共价键
D. Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是NO2和O2形成的原电池装置。下列说法不正确的是
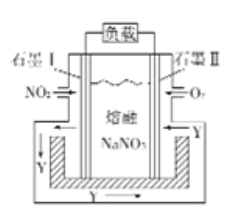
A. 石墨Ⅱ做正极,O2发生还原反应
B. 该电池放电时NO3-从右侧向左侧迁移
C. 当消耗1mol NO2时,电解质中转移1mol e
D. 石墨Ⅰ附近发生的反应为NO2+NO3--e-=N2O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( )

A.该反应的化学方程式为M═2N
B.若t1=1,则反应开始至t1时间段M 的反应速率为1mol﹒L-1﹒min-1
C.t3时正反应速率等于逆反应速率
D.t2时正逆反应速率相等,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
试回答下列问题:
(1)当反应①转移3 mol电子时,消耗H2SO4的质量是______g,产生氢气的体积(标准状况)________L。
(2)反应②中________作氧化剂,________是氧化产物。
(3)当反应②中生成11.2 L SO2气体(标准状况下)时,被还原的H2SO4的物质的量是________。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)__________。
(5)反应③中氧化产物与还原产物的物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表诞生150周年,目前周期表七个周期均已排满,共118种元素,如图是元素周期表短周期的一部分,下列说法中正确的是( )
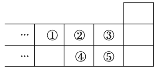
A. 元素①位于第二周期第ⅣA族
B. 气态氢化物的稳定性:④>②
C. 最高价氧化物对应水化物的酸性:⑤>④
D. 元素的最高正化合价:③=⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com