
【题目】某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液。
②按如图连接好装置并加入混合液,用小火均匀加热3~5min。
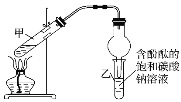
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)配制混合液的操作顺序是___。
(2)装置中球形干燥管,除起冷凝作用外,另一重要作用是___。
(3)步骤②安装好实验装置,加入药品前还应检查___。
(4)写出实验中加热试管的目的:①___;②___。
(5)反应中浓硫酸的作用是__;写出能表示18O位置的制取乙酸乙酯的化学方程式:___。
(6)上述实验中饱和碳酸钠溶液的作用是__。(填字母)
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
D.加速酯的生成,提高其产率
(7)步骤③所观察到的现象是___,从试管乙中分离出乙酸乙酯的实验操作名称是___。
【答案】先加入乙醇(含18O),然后边摇动试管边慢慢加入浓硫酸,冷却后,再加乙酸 防止倒吸 装置的气密性 加快反应速率 及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动 催化剂、吸水剂 CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O BC 试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅 分液
CH3CO18OC2H5+H2O BC 试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅 分液
【解析】
浓硫酸的密度比乙酸、乙醇的密度大,稀释浓硫酸时会放出大量的热;乙酸和乙醇易溶于水,容易引起倒吸;酯化反应的实质是酸去羟基醇去氢。
(1)浓硫酸的密度大于乙酸、乙醇的密度,稀释浓硫酸时会放出大量的热,同时为减少乙醇和乙酸的挥发,所以配制混合液的操作顺序是先加入密度小的乙醇(含18O),然后边摇动试管边慢慢加入浓硫酸,冷却后,再加乙酸;
(2)干燥管的作用:一是起冷凝的作用,二是防倒吸的作用,因为乙酸和乙醇易溶于碳酸钠;
(3)因为产生蒸气,因此加药品前,要检验装置的气密性;
(4)加热试管的目的:①加热,温度升高,能加快反应速率;②乙酸乙酯沸点低,加热时能及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动;
(5)反应中浓硫酸的作用是催化剂:加快反应速率、吸水剂:以利于平衡向生成乙酸乙酯的方向移动;酯化反应的实质是酸去羟基醇去氢,化学方程式为CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;
(6)乙酸乙酯中混有乙酸和乙醇,乙醇易溶于水,乙酸可以和碳酸钠反应,因此碳酸钠的作用是除去乙酸、吸收乙醇、降低乙酸乙酯的溶解度,即选项B C正确;
(7)乙酸乙酯是不溶于水的液体,且密度小于水,现象:试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅;采用分液的方法进行分离。


科目:高中化学 来源: 题型:
【题目】(1)现有氧化还原反应:3H2O2 + 2H2CrO4 =2Cr(OH)3 + 3O2 ↑+ 2H2O
①用单线桥标出反应中的电子转移数目和方向_____________;
②其中Cr被___________,H2O2作___________剂;
③反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,现象是:________;
②在试管中加入少量Na2O2再加入少量水,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,有关化学反应和能量变化的说法正确的是( )
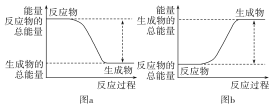
A.a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
B.图b中反应物比生成物稳定
C.图a表示的是吸热反应的能量变化图
D.图a不需要加热就一定能发生,图b一定需要加热才能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) ![]() H2S(g)+CO(g) △H=+7kJ/mol。
H2S(g)+CO(g) △H=+7kJ/mol。
已知:2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol。
写出表示CO燃烧热的热化学方程式:______________。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率____(填“增大”“减小”或“不变”,下同),COS的转化率_______。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5min内,v(H2S)=_______mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A(C2H2)为原料合成食用香料E和吡咯(pyrrole)的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
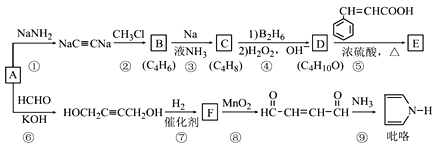
回答下列问题:
(1)A的名称是______;F中含氧官能团的名称是________________。
(2)⑥的反应类型是_____________,⑧的反应类型是_________________。
(3)反应⑤的化学方程式为____________________。
(4)已知C是反式产物,则C的结构简式为_______________。
(5)肉桂酸(![]() )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有________种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2∶3的两组峰的有机物的结构简式是_________。
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有________种(不考虑顺反异构)。与D互为同分异构体,且核磁共振氢谱有面积比为2∶3的两组峰的有机物的结构简式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中正确的是
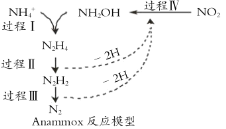
A.1mol NH4+所含的质子总数为 10NA
B.联氨(N2H4)中含有离子键和非极性键
C.过程 II 属于氧化反应,过程 IV 属于还原反应
D.过程 I 中,参与反应的 NH4+ 与 NH2OH 的物质的量之比为 1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
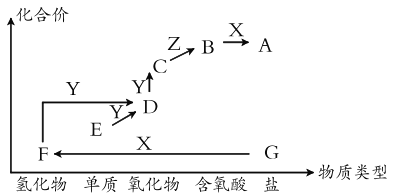
【题目】如图是某元素的价类二维图。其中X是一种强碱,G为正盐,通常条件下Z是无色液体,D的相对原子质量比C小16,各物质转化关系如图所示。下列说法正确的是
A.E 可以是金属也可以是非金属
B.C 和 D 两种大气污染物,都能用排空气法收集
C.B 的浓溶液具有吸水性,可用来干燥气体
D.实验室制备 F 时,可以将其浓溶液滴入碱石灰中进行制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10O2的有机物R在酸性条件下可水解为酸和醇,下列说法不正确的是
A.这些醇和酸重新组合可形成的酯共有40种
B.分子式与R相同的酸与足量碱石灰共热,最多可得到2种烷烃
C.R水解得到的酸至少有5对共用电子对数目
D.R水解得到的醇发生消去反应,可得到4种烯烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com