
| A�� | �������������+3�� | |
| B�� | ʪ����ÿ����1mol Na2FeO4ת��3 mol���� | |
| C�� | �ɷ���ÿ����1mol Na2FeO4ת��4 mol���� | |
| D�� | K2FeO4����ˮʱ������������ɱ������������ˮ�е��������� |
���� A�����ݻ��ϼ۴�����Ϊ0������
B��ʪ����ÿ����1molNa2FeO4����1molFe��OH��3�μӷ�Ӧ�����ݻ��ϼ۵ı仯������
C���ɷ���ÿ����1molNa2FeO4����1molFeSO4�μӷ�Ӧ�����ݻ��ϼ۵ı仯������
D��K2FeO4����ǿ�����ԣ���ԭ����ΪFe3+��Fe3+ˮ������Fe��OH��3���壮
��� �⣺A�����ݻ��ϼ۴�����Ϊ0��ԭ���֪���������������+6�ۣ���A����
B��ʪ����ÿ����1molNa2FeO4����1molFe��OH��3�μӷ�Ӧ�����ϼ���+3�����ߵ�+6�ۣ�ת�Ƶ���3mol����B��ȷ��
C���ɷ���ÿ����1molNa2FeO4����1molFeSO4�μӷ�Ӧ�����ϼ���+2�����ߵ�+6�ۣ�ת�Ƶ���4mol����C��ȷ��
D��K2FeO4����ǿ�����ԣ�����������ɱ��������ԭΪFe3+��ˮ������Fe��OH��3���壬���������ԣ�����������ˮ�е��������ʣ���D��ȷ��
��ѡA��
���� ���⿼��������ԭ��Ӧ����Ŀ�Ѷ��еȣ�ע�ⲻͬ�Ʊ������ķ�Ӧԭ��������Ԫ�ػ��ϼ۵��жϷ������ӻ��ϼ۱仯�ĽǶȷ���������ԭ��Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��58.5 g NaCl����1 Lˮ�пɵ�1 mol•L-1��NaCl��Һ | |
| B�� | ��1 L 1 mol/L��NaCl��Һ��ȡ��10 mL����Ũ������1 mol/L | |
| C�� | �к�100 mL 1 mol/L��H2SO4��Һ�������Σ���NaOH 4 g | |
| D�� | ��78 g Na2O2����ˮ�����1 L��Һ�ɵõ�Ũ��Ϊ1 mol•L-1��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
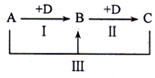 A��B��C��D��ʾ��ѧ��ѧ�е����ֳ������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ�����ַ�Ӧ�е�ˮ����ȥ����
A��B��C��D��ʾ��ѧ��ѧ�е����ֳ������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ�����ַ�Ӧ�е�ˮ����ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2ֱ���� | B�� | CO2ƽ�������� | C�� | BCl3������ | D�� | CH4���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�����ӵ�̼ԭ�ӵĺ��ط��ţ�12C | B�� | HF�ĵ���ʽ�� | ||
| C�� | �Ȼ�þ  | D�� | Cl-���ӵĽṹʾ��ͼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.15 mol/L | B�� | 0.225 mol/L | C�� | 0.35 mol/L | D�� | 0.45 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH��CH+H2O $��_{��}^{HgSO_{4}}$CH3CHO | |
| B�� | C2H5Br+H2O $��_{��}^{NaOH}$ C2H5OH+HBr | |
| C�� | CaC2+2H2O��Ca��OH��2+C2H2�� | |
| D�� | CH3COOCH3+H2O$��_{��}^{����}$CH3COOH+CH3OH |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com