
��10�֣���100��ʱ����0.200 mol�������������������2L��յ��ܱ������У�ÿ��һ��ʱ��Ը������ڵ����ʽ��з������õ����±���
|
ʱ�䣨S�� |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4) |
0.100 |
c1 |
0.050 |
c3 |
a |
b |
|
c(NO2) |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
0.120 |
����գ�
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_________________________________���ﵽƽ��ʱ������������ת����Ϊ________%��
��2��20sʱ������������Ũ��c1=________mol��L-1����0��20sʱ����ڣ�������������ƽ����Ӧ����Ϊ________mol•L-1•s-1��
��3��������ͬ���������������г�����Ƕ����������壬Ҫ�ﵽ����ͬ����ƽ��״̬�����������ij�ʼŨ��Ϊ________mol•L-1��
��10�֣���1��N2O4 2NO2 60 ��2��0.070 0.0015 ��3��0.2
2NO2 60 ��2��0.070 0.0015 ��3��0.2
����������1������ԭ���غ��֪������ʽΪN2O4 2NO2��ƽ��ʱNO2��0.120mol��2L��0.24mol����������N2O4����0.120mol�������ת���ʾ���0.120mol��0.20mol��100����60����
2NO2��ƽ��ʱNO2��0.120mol��2L��0.24mol����������N2O4����0.120mol�������ת���ʾ���0.120mol��0.20mol��100����60����
��2��20sʱNO2��Ũ����0.060mol/L����������N2O4����0.030mol/L�����Դ�ʱ������������Ũ��c1=0.100mol/L��0.030mol/L��0.070mol/L��N2O4�ķ�Ӧ������0.030mol/L��20s��0.0015mol•L-1•s-1��
��3������ƽ�⽨����;����ϵ������Ҫ����ƽ���Ч�������NO2��Ũ��Ӧ����ԭN2O4��2������0.2mol/L��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��100��ʱ����0.40mol���������������2L��յ��ܱ������У�ÿ��һ��ʱ��ͶԸ������ڵ����ʽ��з������õ����±����ݣ�
��100��ʱ����0.40mol���������������2L��յ��ܱ������У�ÿ��һ��ʱ��ͶԸ������ڵ����ʽ��з������õ����±����ݣ�| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��100��ʱ����0.40molNO2�������2L�ܱ������У�ÿ��һ��ʱ��Ը����������ʽ��в������õ����������±���
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �ǽ���Ԫ�ص��ж����������NO��NO2��N2O4�ȣ�
�ǽ���Ԫ�ص��ж����������NO��NO2��N2O4�ȣ�| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
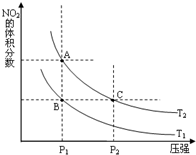 �����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����
�����γɶ����������NO��NO2��N2O4�ȣ�NO2��N2O4�����ת����| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com