
【题目】工业上冶炼铁的原理为:Fe2O3 +3CO![]() 2Fe+ 3CO2。
2Fe+ 3CO2。
(1)该反应中氧化剂是__(填化学式),碳元素被__(填“氧化”或“还原”)。
(2)若消耗了3molCO,则生成CO2的体积是__L(标准状况),转移电子的物质的量是___mol。
【答案】Fe2O3 氧化 67.2 6
【解析】
(1)根据氧化还原反应中元素化合价升降来判断;
(2)根据标况下,V=nVm计算气体体积,根据氧化还原反应中电子得失计算电子的物质的量。
(1)Fe2O3中铁的化合价由+3价变为0价,化合价降低被还原,作氧化剂;CO中碳元素的化合价由+2价变为+4价,化合价升高被氧化,作还原剂;
故答案为:Fe2O3;氧化;
(2)根据反应方程式,若消耗了3molCO同时生成了3molCO2,则标况下,CO2的体积=nVm=3mol×22.4L/mol=67.2L;CO中碳元素的化合价由+2价变为+4价,即1molCO转移2mol电子,则3molCO共转移6mol电子,
故答案为:67.2;6。


 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】瑞德西韦是一种核苷类似物,研究表明它对治疗新冠病毒具有一定的治疗效果, 其中 K 为合成瑞德西韦过程中重要的中间体,其制备方法如下图所示。请回答:

已知:①
②R-OH![]()
(1)下列说法正确的是_____________。
A.化合物D能发生加成、取代、氧化反应,不发生还原反应
B.化合物A能与FeCl3溶液发生显色反应
C.化合物 I 具有两性
D.K的分子式是C20H22N2PO7
(2)写出化合物C的结构简式______________。
(3)写出 F+J→K的化学方程式_____________。
(4)请以苯甲醇为原料合成 的流程_____________。
的流程_____________。
(5)X是C的同分异构体,写出满足下列条件的X的结构简式_____________
①苯环上含有硝基且苯环上只有一种氢原子;
②遇FeCl3溶液发生显色反应;
③1 mol X与足量金属Na反应可生成2 g H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,利用FeCl2、NH4H2PO4、Li2CO3和苯胺(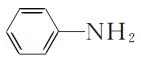 )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
(1)Fe2+基态核外电子排布式为________。
(2) N、P、O三种元素的电负性由大到小的顺序为________。
(3) CO32-中心原子轨道的杂化类型为________;与CO32-互为等电子体的一种分子为________(填化学式)。
(4) 1 mol苯胺分子中含有σ键的数目为________;苯胺与甲苯的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是化学中常用的思维方法。下列推理正确的是
A.lmol晶体硅含Si-Si键的数目为2NA,则1mol金刚砂含C-Si键的数目也为2NA
B.Ca(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式:![]()
则Mg(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式: ![]()
C.标准状况下,22.4 L CO2中所含的分子数目为NA个,则22.4 LCS2中所含的分子数目也为NA个
D.NaClO溶液中通人过量CO2发生了反应:![]() ,则Ca(ClO)2溶液中通入过量CO2发生了:
,则Ca(ClO)2溶液中通入过量CO2发生了:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示,则下列叙述正确的是( )
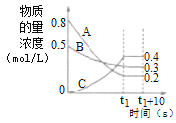
A.该反应的化学方程式为A(g)+3B(g)2C(g)
B.(t1+10)s时,升高温度,正、逆反应速率加快
C.在t1s时,V正(A)=0
D.若该反应在绝热容器中进行,也在t1时刻达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾已经成为部分城市发展的障碍。雾霾形成的最主要原因是人为排放,其中汽车尾气污染对雾霾的“贡献”逐年增加。回答下列问题:
(1)汽车尾气中含有NO,N2与O2生成NO的过程如下:

①1molO2与1molN2的总能量比2molNO的总能量___(填“高”或“低”)。
②N2(g)+O2(g)═2NO(g)的△H=___。
③NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)2CO2(g)+N2(g)△H=akJmol﹣1,但该反应速率很慢,若使用机动车尾气催化转化器,可以使尾气中的NO与CO转化成无害物质排出。上述反应在使用“催化转化器”后,a值___(选填“增大”“减小”或“不变”)。
(2)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1。如图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)═CO2(g)+3H2(g)的△H1___(选填“>”“=”或“<”)0
②图中途径(Ⅱ)的条件是___,途径(Ⅰ)的反应热___(选填“>”“=”或“<”)途径(Ⅱ)的反应热。
③已知下列两个热化学方程式:
2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g)△H2
H2(g)+![]() O2(g)═H2O(g)△H3
O2(g)═H2O(g)△H3
△H1、△H2、△H3三者的关系式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氢氧燃料电池构造示意图。下列说法不正确的是( )

A. a极是负极
B. 电流由b通过灯泡流向a
C. 该电池总反应是2H2+ O2=2H2O
D. b极的电极反应为:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的
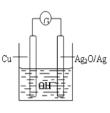
A.Cu为正极,Ag2O为负极
B.电池工作时,OH—向正极移动
C.正极的电极反应为:2Cu+2OH——2e—=Cu2O+H2O
D.外电路中每通过2mol电子,正极质量减少16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100 mL 0.5 mol/L碳酸钠溶液和100 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则关于盐酸的浓度可能是( )
A.0.25 mol/LB.0.5 mol/LC.0.75 mol/LD.1 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com