
把下列四种X溶液分别加入四个盛有10mL 2mol/L的盐酸的烧杯中,同时加水稀释到50mL,此时X和盐酸缓慢反应.其中反应速率最大的是()
A. 10℃20mL3mol/L的X溶液 B. 20℃30mL2mol/L的X溶液
C. 20℃10mL4mol/L的X溶液 D. 10℃10mL2mol/L的X溶液
考点: 化学反应速率和化学计量数的关系.
专题: 化学反应速率专题.
分析: 先计算出稀释后X溶液的中X的物质的量,最后溶液的体积都为50mL,则物质的量越大,浓度越大,则反应速率越大;并结合温度越高,反应速率越大来判断.
解答: 解:A、10℃20mL3mol/L的X溶液,X的物质的量为0.02L×3mol/L=0.06mol;
B、20℃30mL2mol/L的X溶液,X的物质的量为0.03L×2mol/L=0.06mol;
C、20℃10mL4mol/L的X溶液,X的物质的量为0.01L×4mol/L=0.04mol;
D、10℃10mL2mol/L的X溶液,X的物质的量为0.01L×2mol/L=0.02mol,
显然四种情况下B中温度最高,浓度最大,所以反应速率是最大,
故选B.
点评: 本题考查反应速率与温度、浓度的关系及物质的量的计 算,明确影响化学反应速率的因素,物质的量与浓度的关系是解答本题的关键,难度不大.
算,明确影响化学反应速率的因素,物质的量与浓度的关系是解答本题的关键,难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
在c(H+):c(OH﹣)=1:2的水溶液中能大量共存的离子组是()
A. K+、Al3+、HCO3﹣、SO42﹣ B. Ca2+、NH4+、CO32﹣、Cl﹣
C. Na+、K+、NO3﹣、ClO﹣ D. Na+、Fe2+、I﹣、SO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
向10mL 0.1mol•L﹣1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是()
A. x=10时,溶液中有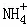 、Al3+、
、Al3+、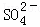 ,且c(
,且c(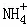 )=c(Al3+)
)=c(Al3+)
B. x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O
C. x=30时,溶液中有Ba2+、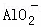 、OH﹣,且c(OH﹣)>c(
、OH﹣,且c(OH﹣)>c(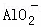 )
)
D. 滴加过程中,生成沉淀的最大物质的量为0.003mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是()
A. 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加
B. 化学反应速率为“0.8mol/(L•s)”表示的意思是:时间为1s时,某物质的浓度为0.8mol/L
C. 根据化学反应速率的大小可以知道化学反应进行的快慢
D. 对于任何化学反应来说,反应速率越大,反应现象越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是()
A. Cu能与浓硝酸反应,而不与浓盐酸反应
B. Cu与浓硝酸反应比与稀硝酸反应快
C. N2与O2在常温、常压下不反应,放电时可反应
D. Fe与浓盐酸反应快,与稀盐酸反应慢
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)⇌cC(g)+dD(g),取a mol A和b mol B置于V L的容器中,1min后,测得容器内A的浓度为x mol•L﹣1,这时B的浓度为( ﹣)mol•L﹣1,C的浓度为 mol•L﹣1.这段时间内反应的平均速率若以物质A的浓度变化来表示,应为 mol•L﹣1•min﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
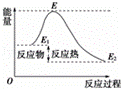
A. 反应物分子(或离子)间的每次碰撞是反应的先决条件
B. 反应物的分子的每次碰撞都能发生化学反应
C. 活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值
D. 活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E﹣E1
查看答案和解析>>
科目:高中化学 来源: 题型:
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是()
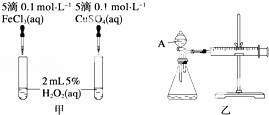
A. 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小
B. 若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C. 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间
D. 为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列热化学方程式分析,C(s)的燃烧热△H等于()
C(s)+H2O(l)=CO(g)+H2(g);△H1=+175.3kJ•mol﹣1
2CO(g)+O2(g)=CO2(g);△H2=﹣566.0kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l);△H3=﹣571.6kJ•mol﹣1.
A. △H1+△H2﹣△H3 B. 2△H1+△H2+△H3
C. △H1+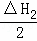 +△H3 D. △H1+
+△H3 D. △H1+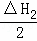 +
+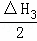
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com