
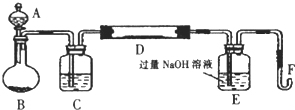
分析 (1)根据装置图可知A、B仪器的名称;
(2)装置中生成的氧气含有水蒸气需要在通入玻璃管前除去水蒸气,选用浓硫酸进行干燥;铁矿石和氧气反应生成氧化铁和二氧化硫,E装置是吸收二氧化硫气防止污染环境;
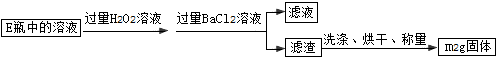
(3)Ⅱ中加入过量H2O2溶液发生的反应是过氧化氢氧化亚硫酸根离子生成硫酸根离子,过氧化氢被还原为水;
(4)依据配制一定体积溶液的操作步骤分析,需要在250mL容量瓶中配制,滴定终点时溶液会出现浅红色;
(5)样品质量为m1g,依据流程分析可知得到硫酸钡沉淀为m2g,依据硫元素守恒计算硫元素质量得到硫元素的质量分数;
解答 解:(1)根据装置图可知A仪器的名称为分液漏斗,B仪器的名称为圆底烧瓶,
故答案为:分液漏斗;圆底烧瓶;
(2)装置中生成的氧气含有水蒸气需要在通入玻璃管前除去水蒸气,选用浓硫酸进行干燥;铁矿石和氧气反应生成氧化铁和二氧化硫,E装置是吸收二氧化硫气防止污染环境;
故答案为:浓硫酸;吸收二氧化硫;
(3)Ⅱ中加入过量H2O2溶液发生的反应是过氧化氢氧化亚硫酸根离子生成硫酸根离子,过氧化氢被还原为水,反应的离子方程式为:H2O2+SO32-═SO42-+H2O;
故答案为:H2O2+SO32-═SO42-+H2O;
(4)依据配制一定体积溶液的操作步骤分析,需要在250mL容量瓶中配制,滴定终点的标志是当滴入最后一滴酸性KMnO4标准液时,溶液出现浅红色,且30S内不复原,
故答案为:250mL容量瓶;当滴入最后一滴酸性KMnO4标准液时,溶液出现浅红色,且30S内不复原;
(5)样品质量为m1g,依据流程分析可知得到硫酸钡沉淀为m2g,硫元素物质的量=硫酸钡物质的量=$\frac{m{\;}_{2}g}{233g/mol}$=$\frac{m{\;}_{2}}{233}$mol;依据硫元素守恒计算硫元素质量得到硫元素的质量分数=$\frac{\frac{m{\;}_{2}}{233}mol×32g/mol}{m{\;}_{1}g}$×100%=$\frac{32m{\;}_{2}}{233m{\;}_{1}}$×100%,
故答案为:$\frac{32m{\;}_{2}}{233m{\;}_{1}}$×100%.
点评 本题考查了物质性质的实验探究方法和实验分析判断,过程中的定量计算关系是解题关键,题目难度中等.


科目:高中化学 来源:2017届河南省高三上第一次联考化学试卷(解析版) 题型:选择题
四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X 的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是()
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于15% | B. | 大于15% | C. | 小于15% | D. | 无法估算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{V}_{1}}{{V}_{2}}$c mol•L-1 | B. | $\frac{{V}_{1}}{{V}_{2}}$c mol•L-1 | ||
| C. | $\frac{{3V}_{2}}{{V}_{1}}$c mol•L-1 | D. | $\frac{3{V}_{1}}{{V}_{2}}$c mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2}$lg($\frac{b}{a}$) | B. | $\frac{1}{2}$lg($\frac{a}{b}$) | C. | 14+$\frac{1}{2}$lg($\frac{a}{b}$) | D. | 14+$\frac{1}{2}$lg($\frac{b}{a}$) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期I B族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615,D-O:348 | 216 | 195 |
 ,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.
,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$. ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com