
���� ��1���÷�ӦΪ�����������Ŀ��淴Ӧ��ѹǿ��Ӱ�컯ѧƽ�⣻
��2��ά������������¶Ȳ��䣬�ﵽƽ��ʱC��Ũ����Ϊ1.2mol/L��Ϊ��Чƽ�⣬��Ϊ��ȫ��Чƽ�⣬����ѧ������ת�����������2molA��1molB��
��� �⣺��1����С����������൱������ѹǿ�����ڸ÷�ӦΪ�����������ķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ���
�ʴ�Ϊ������
��2�����ݵ�Чƽ�⣬�Ѹ����ʶ�����ɷ���ʽ��ߵ����ʣ����ʼ�����2molA��1molB��ȼ��ɣ�
A.4mol A+2mol B ���ʼ2mol A��1molB��ͬ�������ڵ�Чƽ�⣬��A����
B.3molC+l mol D�����A��B����A��BŨ�ȷֱ�Ϊ2mol��1mol�����ʼŨ����ͬ����B��ȷ��
C.2mol A+1mol B+1mol D������DΪ��̬����Ӱ�컯ѧƽ�⣬����ԭ��Ӧ��2mol A��1molB��Ϊ��Чƽ�⣬�ﵽƽ��ʱC��Ũ����ȻΪ1.2mol/L����C��ȷ��
�ʴ�Ϊ��BC��
���� ���⿼���˵�Чƽ���Ӱ�졢��Чƽ����жϼ�Ӧ�ã���Ŀ�Ѷ��еȣ�ע�����յ�Чƽ������ͼ��жϷ�������ȷ��ѧƽ�⼰��Ӱ�����أ���������ע��D��״̬Ϊ���壬Ϊ�״��㣮


 ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 25��ʱ����֪��
25��ʱ����֪��| A�� | W ����ʾ����Һ�У�c��Na+��+c��H+��=2c��CO32-��+c��OH-��+c��HCO3-�� | |
| B�� | pH=4 ����Һ�У�c��H2CO3��+c��HCO3-��+c��CO32-��=0.1 mol•L-1 | |
| C�� | pH=8 ����Һ�У�c��H+��+c��H2CO3��+c��HCO3-��=c��OH-��+c��Cl-�� | |
| D�� | pH=11 ����Һ�У�CO32-+H2O HCO3-+OH- K��1.8��l0-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ�ٺ͢ڶ������ӷ�Ӧ | B�� | ��Ӧ�ٺ͢ڶ��������� | ||
| C�� | ��Ӧ�ٺ͢ڶ��ų����� | D�� | ��Ӧ�ۼȲ���������Ҳ���ų����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Al3+����Һ�У�K+��Na+��NO3-��CO32-���ܴ������棬����Al2��CO3��3�������� | |
| B�� | ������Fe3+����Һ�У�K+Mg2+��I-��Br2-���ܴ������棬��2Fe3++2I-=2Fe2++I2 | |
| C�� | ��ˮ�����c��H+��=1��10-14mol/L����Һ�У�Ca2+��NO3-��HCO3-��Cl-���ܴ������棬����Һ�����ԣ���HCO3-��Ӧ����CO2���� | |
| D�� | ��NH4Fe��SO4��2��Һ�У�Na+��K+��S2-��SCN-���ܴ������棬ֻ����Fe3+��S2-��Ӧ��������ɫ��S���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
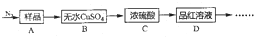
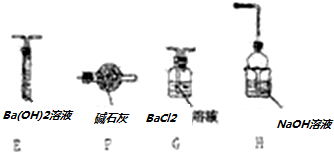
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
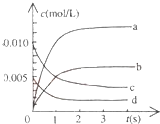 ��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ټӵ����ʵ�����ƿ��ȥ | B�� | Ӱ�첻���ٴ��� | ||
| C�� | �ý�ͷ�ι�ȷ���������ϵ���Һ | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۺ���ά�ض����ã�C6H10O5��n��ʾ������Ϊͬ���칹�� | |
| B�� | Mg5��Si4O10��2��OH��2•4H2O����������ʽ��5MgO•8SiO2•5H2O | |
| C�� | Fe-2e-=Fe2+�ɱ�ʾ�������ⸯʴ��������ʴ��������Ӧ | |
| D�� | �Ҵ����ӵı���ģ�ͣ�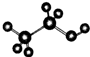 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȡ����ʱ������ѡ��CCl4��ƾ���Ϊ��ȡ���ӵ�ˮ����ȡ�� | |
| B�� | ��������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ���� | |
| C�� | ��Һ����ʱ���²�Һ��ӷ�Һ©���¿ڷų����ϲ�Һ����¿ڷų�����һ���ձ��� | |
| D�� | �������ʱ���ռ�����ֺ���ֹͣ���ȣ����ָ����º���ֹͣͨ����ˮ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com