

 .
.分析 根据元素在周期表中的位置知①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl,
(1)⑧为S元素,原子序数为、核外电子总数都是16,据此画出其原子结构示意图;
(2)原子电子层数越多其原子半径越大,电子层相同时核电荷数越大原子半径越小;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强;
(4)④为O,⑤为Na,二者形成的阴、阳离子个数比为1:2化合物氧化钠;
(5)⑥的单质与①、④、⑤三种元素形成化合物的水溶液反应,生成偏铝酸钠和氢气;
(6)根据C、N、S、Si的单质以及化合物之间的性质来回答.
解答 解:根据元素在周期表中的位置知①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl,
(1)⑧为S,原子序数为=核外电子总数=16,其原子结构示意图为: ,故答案为:
,故答案为: ;
;
(2)原子电子层数越多其原子半径越大,则O的原子半径最小;Na、Al原子都含有3个电子层,Al的核电荷数较大,则原子半径Na>Al,所以原子半径大小顺序是Na>Al>O,
故答案为:Na>Al>O;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性N>C>Si,所以其最高价氧化物的水化物酸性HNO3>H2CO3>H2SiO3,
故答案为:HNO3>H2CO3>H2SiO3;
(4)④为O,⑤为Na,O、Na形成的阴、阳离子个数比为1:2化合物为氧化钠,化学式为Na2O,
故答案为:Na2O;
(5)⑥的单质为Al,①、④、⑤三种元素形成化合物为NaOH,铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)将C、N、S、Si代入单质$\stackrel{④单质}{→}$化合物1$\stackrel{④单质}{→}$化合物2$\stackrel{H_{2}O}{→}$最高价氧化物对应的水化物转化关系中,只有Si不成立,则符合转化关系的是C、N、S,
故答案为:C、N、S.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素化合物性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
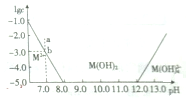
| A. | M(OH)2属于两性氢氧化物 | |
| B. | 沉淀分离M2+需控制pH在8~12之间 | |
| C. | 升高温度,可以实现从b点移动到a点 | |
| D. | 室温时,M(OH)2(s)的溶度积常数为1×10-17 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
| A(g) | B2(g) | C(g) | C(g) | ||
| Ⅰ | 500 | 0.5 | 1.0 | 0 | 0.4 |
| Ⅱ | 500 | a | b | 0.25 | 0.4 |
| Ⅲ | 600 | 0.25 | 0.5 | 0.25 | 0.35 |
| A. | 容器Ⅰ中的反应在前5 min的平均反应速率v(A)=0.08 mol•L-1•min-1 | |
| B. | 该反应的正反应为放热反应 | |
| C. | 容器Ⅱ中起始时a=0.25,b=0.5 | |
| D. | 若起始时向容器Ⅰ中加入A 0.8 mol、B2 1.6 mol,达到平衡时A的转化率为80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14种 | B. | 12种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第三次调研化学试卷(解析版) 题型:选择题
臭氧在烟气脱硝中的反应为2NO2(g)+O2(g) N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com