
��ҵ�Ϻϳɰ���һ�������½������·�Ӧ��N2��g��+3H2��g��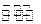 2NH3��g�� ��H=-92��44 kJ��mol���䲿�ֹ�����������ͼ��ʾ��
2NH3��g�� ��H=-92��44 kJ��mol���䲿�ֹ�����������ͼ��ʾ��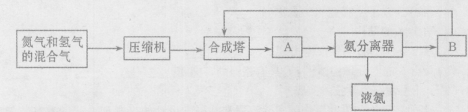
��1���ϳɰ�����Ҫ��ԭ�����У�����ȡ�� ��������Դ�� ��
��2����ԭ�������о���������Ŀ���� ��
��3���豸A�������� ���豸B�������� ��
��4����20��50 Mpaʱ����ҵ�ϳɰ�ѡ����400��500����¶Ƚ��з�Ӧ��
��Ҫԭ���� ��
��5���ݡ���ѧ����־������ϣ����ѧ���ڳ�ѹ�½�������������ϡ�͵ĵ����ֱ�ͨ��һ�����ȵ�570��ĵ��أ���ͼ���У���͵��ڵ缫�Ϻϳ��˰�����ת���ʴﵽ��78������������ӦΪ  ��������ӦΪ ��
��������ӦΪ ��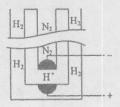

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ���¸�ѹ |
| ||
| ���¸�ѹ |
 CO��g��+3H2��g������H=+QkJ/mol��Q��0��
CO��g��+3H2��g������H=+QkJ/mol��Q��0��| ʱ��/min | CH4��mol�� | H20�� mol�� | CO ��mol�� | H2 ��mol�� |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ��Ϫһ��2010��2011ѧ��߶���ѧ�����п��Ի�ѧ���� ���ͣ�022
�ϳɰ��Ի�ѧ��ҵ������ҵ������Ҫ���壮
(1)
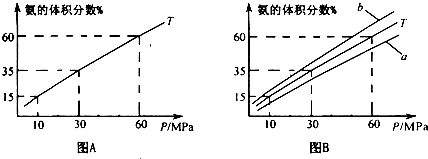
��ϳ����а�1��4����������֮�ȳ���N2��H2���а��ĺϳɣ�ͼAΪT��ʱƽ�������а��������������ѹǿ(P)�Ĺ�ϵͼ��
��д����ҵ�Ϻϳɰ��Ļ�ѧ����ʽ________��
��ͼ
A�а������������Ϊ15.00��ʱ��H2��ת���ʣ�________����ͼB��T��
500�����¶�Ϊ450����Ӧ��������________(ѡ����ĸ��a"��b��)��ѡ���������________������ͼ��֪������ѹǿ�����ԭ�ϵ������ʣ�������ʵ�ʿ�������ѹǿ������������________(д��һ������)��
(2)
�ϳɰ�������������ɼ�����ˮ��Ӧ�Ƶã���Ӧ���Ȼ�ѧ����ʽΪ��![]()
(3)
һ���¶��£���2 L�����з���������Ӧ�������ʵ����ʵ����仯���±�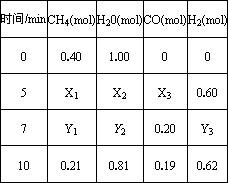
�ٷ����������ݣ��ж�5��7
min֮�䷴Ӧ�Ƿ���ƽ��״̬________(��ǡ���)��ǰ5 minƽ����Ӧ����v(CH4)��________���ڷ�Ӧ��7��10
min֮����CO�����ʵ������ٵ�ԭ�������________(����ĸ)��a��
����CH4b��
�����¶�c��
����ѹǿd��
����H2��
�������¶Ȳ�������1 L��������ʼ����0.15 mol��CH4��0.45 mol��H2O��________mol��CO��________mol��H2���ﵽƽ��ʱCH4������ٷֺ������һ��Ͷ����ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

| ʱ��/min | CH4��mol�� | H20�� mol�� | CO ��mol�� | H2 ��mol�� |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���㽭ʡ������Ϫһ�и߶����£����л�ѧ�Ծ��������棩 ���ͣ������

 CO��g��+3H2��g������H=+QkJ/mol��Q��0��
CO��g��+3H2��g������H=+QkJ/mol��Q��0��| ʱ��/min | CH4��mol�� | H20�� mol�� | CO ��mol�� | H2 ��mol�� |
| 0.40 | 1.00 | |||
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(15 �֣�
�ϳɰ��Ի�ѧ��ҵ������ҵ������Ҫ���塣
(1) ��ϳ����а�1:4�����ʵ���֮�ȳ���N2��H2���а��ĺϳɣ�ͼAΪT0Cʱƽ�������а��������������ѹǿ(P)�Ĺ�ϵͼ��

��д����ҵ�Ϻϳɰ��Ļ�ѧ����ʽ_____________________��
��ͼA�а������������Ϊ15.00%ʱ��H2��ת����=_______ ��
��ͼB��T=5000C���¶�Ϊ4500C��Ӧ��������_______(ѡ����ĸ��a"��b ������ѡ���������______________
����ͼ��֪������ѹǿ�����ԭ�ϵ������ʣ�������ʵ�ʿ�������ѹǿ������������_______(д��һ�����ɣ���
(2) �ϳɰ�������������ɼ�����ˮ��Ӧ�Ƶ�,��Ӧ���Ȼ�ѧ����ʽΪ��
![]()
(3) һ���¶��£���2 L�����з���������Ӧ�������ʵ����ʵ����仯���±�
| ʱ��/min | CH4(mol) | H20( mol) | CO (mol) | H2 (mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com