
| A.三者都是强酸,其稀溶液中只有稀硝酸与铜在常温反应 |
B.浓盐 酸制氯气,浓硫酸使纸张变黑,浓硝酸常温与铜反应,体现了三 酸制氯气,浓硫酸使纸张变黑,浓硝酸常温与铜反应,体现了三 者的强氧化性 者的强氧化性 |
| C.将强氧化性的浓硫酸与浓硝酸按比例混合可以得到氧化性更强的王水 |
| D.铝、铁在冷的浓硫酸或浓硝酸的钝化属于化学反应 |
科目:高中化学 来源:不详 题型:单选题
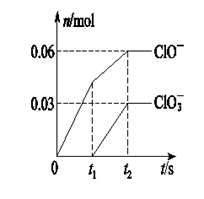
| A.苛性钾溶液中KOH的质量是4.94 g |
| B.反应中转移电子的物质的量是0.09 mol |
| C.氧化性ClO-<ClO |
| D.ClO的生成是由于温度升高引起的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.沾有酚酞的试纸 | B.湿润的碘化钾淀粉试纸 |
| C.沾有氢氧化钠浓溶液的试纸 | D.观察瓶内气体颜色的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 MnCl2+Cl2↑+2H2O)
MnCl2+Cl2↑+2H2O)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
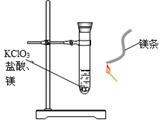
| A.制取氢气并检验其纯度 | B.制取氯气并检验其纯度 |
| C.验证氯酸钾的氧化性 | D.验证光对氢气和氯气反应的作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ClO4-、Cl-、Na+ | B.ClO-、Cl-、H+ |
| C.NaClO、NaClO3 | D.NaClO、NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com