
����Ŀ���ش��������⣺
��1����֪25��ʱNH3��H2O��Kb=2.0 10-5
����0.10 mol/L�� NH3��H2O��c(OH-)=______________mol/L
���������м������NH4Cl��ʹc(NH4+)��Ũ�ȴﵽ0.20 mol/L����c(OH-)=________mol/L
��25��ʱ����a molL-1�İ�ˮ��0.01molL-1�������������������Ϻ���Һ��pH��7���ú�a�Ĵ���ʽ��ʾNH3H2O�ĵ��볣��Kb= ___________________ ��
��2��25��ʱ��0.10molL��1��HA��Һ��c��H+��/c��OH����=1010��
�ٸ�HA��Һ��pH=________��
��25��ʱ������Ũ�ȵ�����İ�ˮ��HA��Һ����, �û����Һ��pH________7������������������������=����
���𰸡� 1.410-3 ��![]() 10-3 1 10-5
10-3 1 10-5 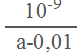 2 ��
2 ��
����������1����NH3H2ONH4++OH-��![]() ��Kb=2.0 ��10-5��Kb=
��Kb=2.0 ��10-5��Kb=![]() =
=![]() =2.0 ��10-5��
=2.0 ��10-5��![]() =
=![]() ��10-3mol/L=1.4��10-3mol/L����Kb=
��10-3mol/L=1.4��10-3mol/L����Kb=![]() =
=![]() =2.0 ��10-5����ã�
=2.0 ��10-5����ã�![]() = 1 ��10-5 mol/L������25���£�ƽ��ʱ��Һ��c��NH4+��=c��Cl-��=0.005mol/L�����������غ��n��NH3H2O��=��0.5a-0.005��mol/L�����ݵ���غ��c��H+��=c��OH-��=10-7mol/L����Һ�����ԣ�NH3H2O�ĵ��볣��Kb=
= 1 ��10-5 mol/L������25���£�ƽ��ʱ��Һ��c��NH4+��=c��Cl-��=0.005mol/L�����������غ��n��NH3H2O��=��0.5a-0.005��mol/L�����ݵ���غ��c��H+��=c��OH-��=10-7mol/L����Һ�����ԣ�NH3H2O�ĵ��볣��Kb=![]() =
=![]() =
=![]() ����2���ٳ����£�ˮ�����ӻ�Kw=c��H+��c��OH-��=10-14����
����2���ٳ����£�ˮ�����ӻ�Kw=c��H+��c��OH-��=10-14����![]() =1010�����c��H+��=10-2mol/L����pH=2����0.10molL��1��HA��ҺpH=2��֤��ΪHA���ᣬ25��ʱ������Ũ�ȵ�����İ�ˮ��HA��Һ���ϣ�������ҺΪNH4A��Һ�����ڣ�Kb=2.0 ��10-5��Ka=
=1010�����c��H+��=10-2mol/L����pH=2����0.10molL��1��HA��ҺpH=2��֤��ΪHA���ᣬ25��ʱ������Ũ�ȵ�����İ�ˮ��HA��Һ���ϣ�������ҺΪNH4A��Һ�����ڣ�Kb=2.0 ��10-5��Ka=![]() =
=![]() =10-3��Kb< Ka,��HA��ĵ������NH3��H2O�ĵ��룬NH4A��Һ�����ԣ�pH��7��
=10-3��Kb< Ka,��HA��ĵ������NH3��H2O�ĵ��룬NH4A��Һ�����ԣ�pH��7��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·�����Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᡣʵ������һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ������˵����ȷ����

A. �������У�������������ԭ��Ӧ
B. ������ӦCH3CHO+2e-+H2O=CH3COOH+2H+
C. �����ܷ�Ӧ����ʽΪ2CH3CHO+H2O=CH3COOH+CH3CH2OH
D. ����CH4--����ȼ�ϵ��Ϊֱ����Դ��ȼ�ϵ�ص�b��Ӧͨ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(-C3H7))�Ķ��ȴ��ﹲ��(���������칹)( )
A.9��B.7��C.8��D.10��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫���������Һ��һ��ʱ����ټ���һ����������һ�����У������ڣ�����Һ����ԭ����Һ��ȫһ�����ǣ� ��
A.AgNO3 ��Ag2O��
B.NaOH��NaOH��
C.NaCl �����ᣩ
D.CuSO4��Cu��OH��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȡ��ˮ��Һ�������ʡ����ᡢ��Ρ�����ȣ���˱��㷺Ӧ���ڻ������Ṥ�����ʡ���ҩ���ϳ���ά�����ϵ���ҵ�У�������Ҫ�Ļ��� ��Ʒ֮һ��
(1) ��ҵ������Ϊԭ���Ʊ�����ĵ�һ���Ļ�ѧ����ʽ____________��
(2) �Լ���Ϊԭ�Ͽ��Ƶ�������ͼ1��һ��������CH4(g)��H2O(g) ��Ӧ����CO(g) ��2molH2(g)�������仯ʾ��ͼ��д�����Ȼ�ѧ����ʽ____________(��H��E1��E2��E3��ʾ)��
(3) ��֪N2(g)+3H2 (g)![]() 2NH3(g) ��H =-94.4kJ/mol����2L�����ܱ������У�������Ũ����ʱ��仯��������ͼ2��ʾ����ʱ������վ���ƽ��״̬��
2NH3(g) ��H =-94.4kJ/mol����2L�����ܱ������У�������Ũ����ʱ��仯��������ͼ2��ʾ����ʱ������վ���ƽ��״̬��
�� ʱ��I �ų�������Ϊ__________��
��25minʱ��ȡ��ij�ִ�ʩ��__________��
��ʱ���������·�Ӧ��ƽ��ʱƽ�ⳣ��K��ֵΪ__________ (������ʽ��ʾ)���ڸ������£�ijʱ�̲����������0.5molN2��1.5molH2��1.0mol NH3,��ʱv��(H2) _____V��(H2) (����<������>������=��)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.1mol/L K2CO3��Һ�У���ʹc��CO32�������ӽ�0.1mol/L���ɲ�ȡ�Ĵ�ʩ�ǣ� ��
A.������������
B.��ˮ
C.��KOH����
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�ҹ���������ʵ���������ദ��������Ĥ������ϩ���������ɵ�طֱ�����������������
A.������������������B.�����������ɻ�������
C.�к���������������D.�ɻ����������к�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������Fe��FeO��Fe2O3�Ļ�����м���120mL 4mol/L��ϡ���ᣬǡ��ʹ�������ȫ�ܽ⣬�ų�1.344LNO����״��������������Һ�м���KSCN��Һ����ɫ���֣�����������CO�ڼ����»�ԭ��ͬ�����Ļ������յõ��������ʵ���Ϊ�� ��
A.0.21mol
B.0.24mol
C.0.16mol
D.0.14mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���������ȷ����
A.������Cu(OH)2�м���������Һ�����ȣ����ֺ�ɫ����
B.��FeCl3��Һ�м�������ͭ�ۣ�ͭ���ܽ�
C.�����£���Ũ�����м�����Ƭ����Ƭ�ܽ�
D.������Һ�м��뱥��(NH4)2SO4��Һ�����ְ�ɫ������������������ˮ���������ܽ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com